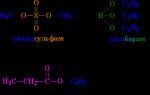Vetitë fizike të estereve. Nomenklatura dhe izomeria
Nëse acidi fillestar është polibazik, atëherë formimi i ose estereve të plota është i mundur - të gjitha grupet HO zëvendësohen, ose esteret e acidit - zëvendësimi i pjesshëm. Për acidet monobazike janë të mundshme vetëm esteret e plota (Fig. 1).
Oriz. 1. SHEMBUJ ESTERësh me bazë acidin inorganik dhe karboksilik
Nomenklatura e estereve.
Emri krijohet si më poshtë: fillimisht tregohet grupi R i lidhur me acidin, pastaj emri i acidit me prapashtesën "at" (si në emrat e kripërave inorganike: karboni në natriumi, nitrat në krom). Shembuj në Fig. 2

Oriz. 2. EMRAT E ESTREVE. Fragmentet e molekulave dhe fragmentet përkatëse të emrave janë theksuar me të njëjtën ngjyrë. Esteret zakonisht mendohen si produkte reagimi midis një acidi dhe një alkooli; për shembull, propionati i butilit mund të mendohet si rezultat i reagimit midis acidit propionik dhe butanolit.
Nëse përdorni të parëndësishme ( cm. EMRAT TRIVIALE TË SUBSTANCAVE) emri i acidit fillestar, pastaj emri i përbërjes përfshin fjalën "ester", për shembull, C 3 H 7 COOC 5 H 11 - amil ester i acidit butirik.
Klasifikimi dhe përbërja e estereve.
Ndër esterët e studiuar dhe të përdorur gjerësisht, shumica janë komponime që rrjedhin nga acidet karboksilike. Esteret e bazuara në acide minerale (inorganike) nuk janë aq të ndryshme, sepse klasa e acideve minerale është më pak e madhe se acidet karboksilike (larmia e përbërjeve është një nga shenjat dalluese të kimisë organike).
Kur numri i atomeve C në acidin karboksilik origjinal dhe alkoolin nuk i kalon 6-8, esterët përkatës janë lëngje vajore pa ngjyrë, më së shpeshti me erë frutash. Ata formojnë një grup esterësh frutash. Nëse një alkool aromatik (që përmban një bërthamë aromatike) është i përfshirë në formimin e një esteri, atëherë komponime të tilla, si rregull, kanë një erë lulesh dhe jo frutash. Të gjitha komponimet në këtë grup janë praktikisht të patretshme në ujë, por lehtësisht të tretshëm në shumicën e tretësve organikë. Këto komponime janë interesante për shkak të gamës së tyre të gjerë të aromave të këndshme (Tabela 1); disa prej tyre fillimisht u izoluan nga bimët dhe më vonë u sintetizuan artificialisht.
| Tabela 1. DISA ESTRE, me një aromë frutash ose lulesh (fragmentet e alkooleve origjinale në formulën e përbërjes dhe në emër janë të theksuara me shkronja të zeza) | ||
| Formula e Esterit | Emri | Aroma |
| CH 3 COO C 4 H 9 | Butil acetat | dardhë |
| C 3 H 7 COO CH 3 | Metil Ester i acidit butirik | mollë |
| C 3 H 7 COO C 2 H 5 | Etil Ester i acidit butirik | ananasi |
| C 4 H 9 COO C 2 H 5 | Etil | i kuq |
| C 4 H 9 COO C 5 H 11 | Isoamili ester i acidit izovalerik | banane |
| CH 3 COO CH 2 C 6 H 5 | Benzil acetat | jasemini |
| C 6 H 5 COO CH 2 C 6 H 5 | Benzil benzoat | me lule |
Kur madhësia e grupeve organike të përfshira në estere rritet në C 15-30, komponimet fitojnë konsistencën e substancave plastike, lehtësisht të zbutura. Ky grup quhet dyllë; ata zakonisht janë pa erë. Dylli i bletës përmban një përzierje esteresh të ndryshëm; një nga përbërësit e dyllit, i cili u izolua dhe u përcaktua përbërja e tij, është esteri myricil i acidit palmitik C 15 H 31 COOC 31 H 63. Dylli kinez (produkt i sekretimit të kokinit - insektet e Azisë Lindore) përmban ester ceril të acidit cerotik C 25 H 51 COOC 26 H 53. Përveç kësaj, dyllërat përmbajnë gjithashtu acide karboksilike dhe alkoole të lira, të cilat përfshijnë grupe të mëdha organike. Dyllët nuk lagen nga uji dhe janë të tretshëm në benzinë, kloroform dhe benzinë.
Grupi i tretë janë yndyrnat. Ndryshe nga dy grupet e mëparshme të bazuara në alkoolet monohidrike ROH, të gjitha yndyrat janë estere të formuara nga glicerina e alkoolit trihidrik HOCH 2 – CH (OH) – CH 2 OH. Acidet karboksilike që përbëjnë yndyrnat zakonisht kanë një zinxhir hidrokarburesh me 9-19 atome karboni. Yndyrnat shtazore (gjalpi i lopës, qengji, sallo) janë substanca plastike, të shkrirë. Yndyrnat bimore (ulliri, farat e pambukut, vaji i lulediellit) janë lëngje viskoze. Yndyrnat shtazore kryesisht përbëhen nga një përzierje e glicerideve të acidit stearik dhe palmitik (Fig. 3A, B). Vajrat vegjetale përmbajnë gliceride acidesh me një gjatësi zinxhiri karboni pak më të shkurtër: laurik C 11 H 23 COOH dhe miristik C 13 H 27 COOH. (si acidet stearik dhe palmitik, këto janë acide të ngopura). Vajra të tillë mund të ruhen në ajër për një kohë të gjatë pa ndryshuar konsistencën e tyre, dhe për këtë arsye quhen jo-tharëse. Në të kundërt, vaji i farave të lirit përmban glicerid të pangopur të acidit linoleik (Figura 3B). Kur aplikohet në një shtresë të hollë në sipërfaqe, vaji i tillë thahet nën ndikimin e oksigjenit atmosferik gjatë polimerizimit përgjatë lidhjeve të dyfishta dhe formohet një film elastik që është i pazgjidhshëm në ujë dhe tretës organikë. Vaji natyral i tharjes është bërë nga vaji i lirit.

Oriz. 3. GLICERIDET E ACIDEVE stearik dhe palmitik (A DHE B)– përbërësit e yndyrës shtazore. Gliceridi i acidit linoleik (B) është një përbërës i vajit të lirit.
Esteret e acideve minerale (sulfatet alkil, boratet alkil që përmbajnë fragmente të alkooleve më të ulëta C 1-8) janë lëngje vajore, esteret e alkooleve më të larta (duke filluar nga C 9) janë komponime të ngurta.
Vetitë kimike të estereve.
Më karakteristikë e estereve të acideve karboksilike është ndarja hidrolitike (nën ndikimin e ujit) e lidhjes esterike; në një mjedis neutral ajo vazhdon ngadalë dhe përshpejtohet dukshëm në prani të acideve ose bazave, sepse Jonet H + dhe HO – e katalizojnë këtë proces (Fig. 4A), me jonet hidroksil që veprojnë në mënyrë më efikase. Hidroliza në prani të alkaleve quhet saponifikimi. Nëse merrni një sasi alkali të mjaftueshme për të neutralizuar të gjithë acidin e formuar, atëherë ndodh saponifikimi i plotë i esterit. Ky proces kryhet në shkallë industriale dhe glicerina dhe acidet karboksilike më të larta (C 15–19) fitohen në formën e kripërave të metaleve alkali, të cilat janë sapuni (Fig. 4B). Fragmentet e acideve të pangopura që përmbahen në vajrat bimore, si çdo përbërje e pangopur, mund të hidrogjenizohen, hidrogjeni ngjitet në lidhje të dyfishta dhe formohen përbërje të ngjashme me yndyrat shtazore (Fig. 4B). Duke përdorur këtë metodë, yndyrat e ngurta prodhohen industrialisht me bazë vaji të lulediellit, sojës ose misrit. Margarina është bërë nga produktet e hidrogjenizimit të vajrave bimore të përziera me yndyrna natyrore shtazore dhe aditivë të ndryshëm ushqimorë.

Metoda kryesore e sintezës është ndërveprimi i një acidi karboksilik dhe një alkooli, i katalizuar nga acidi dhe i shoqëruar me lëshimin e ujit. Ky reagim është i kundërt me atë të treguar në Fig. 3A. Në mënyrë që procesi të vazhdojë në drejtimin e dëshiruar (sinteza e esterit), uji distilohet (distilohet) nga përzierja e reaksionit. Nëpërmjet studimeve speciale duke përdorur atome të etiketuara, u arrit të vërtetohej se gjatë procesit të sintezës, atomi O, i cili është pjesë e ujit që rezulton, shkëputet nga acidi (i shënuar me një kornizë me pika të kuqe), dhe jo nga alkooli ( opsioni i parealizuar theksohet me një kornizë blu me pika).
Duke përdorur të njëjtën skemë, fitohen esteret e acideve inorganike, për shembull, nitroglicerina (Fig. 5B). Në vend të acideve, mund të përdoren kloruret acide; metoda është e zbatueshme si për acidet karboksilike (Fig. 5C) dhe ato inorganike (Fig. 5D).
Ndërveprimi i kripërave të acidit karboksilik me halogjenët RCl gjithashtu çon në estere (Fig. 5D); reagimi është i përshtatshëm në atë që është i pakthyeshëm - kripa inorganike e lëshuar hiqet menjëherë nga mjedisi i reaksionit organik në formën e një precipitati.
Përdorimi i estereve.
Formati etilik HCOOC 2 H 5 dhe acetati etilik H 3 COOC 2 H 5 përdoren si tretës për llaqet e celulozës (në bazë të nitrocelulozës dhe acetatit të celulozës).
Esteret e bazuara në alkoole dhe acide më të ulëta (Tabela 1) përdoren në industrinë ushqimore për të krijuar esenca frutash, dhe esteret me bazë alkoolet aromatike në industrinë e parfumeve.
Lubrifikuesit, lubrifikantët, kompozimet ngopëse për letër (letër dylli) dhe lëkurë janë bërë nga dylli; ato përfshihen gjithashtu në kremrat kozmetikë dhe pomadat medicinale.
Yndyrnat, së bashku me karbohidratet dhe proteinat, përbëjnë një grup ushqimesh të nevojshme për të ushqyer; ato janë pjesë e të gjitha qelizave bimore dhe shtazore; përveç kësaj, kur grumbullohen në trup, ato luajnë rolin e një rezerve energjie. Për shkak të përçueshmërisë së saj të ulët termike, shtresa e yndyrës mbron mirë kafshët (veçanërisht kafshët detare - balenat ose detet) nga hipotermia.
Yndyrnat shtazore dhe bimore janë lëndë të para për prodhimin e acideve karboksilike më të larta, detergjentëve dhe glicerinës (Fig. 4), të përdorura në industrinë kozmetike dhe si përbërës të lubrifikantëve të ndryshëm.
Nitroglicerina (Fig. 4) është një ilaç dhe eksploziv i njohur, baza e dinamitit.
Vajrat tharëse bëhen nga vajra bimore (Fig. 3), të cilat përbëjnë bazën e bojrave të vajit.
Esteret e acidit sulfurik (Fig. 2) përdoren në sintezën organike si reagentë alkilues (duke futur një grup alkil në një përbërje), dhe esteret e acidit fosforik (Fig. 5) përdoren si insekticide, si dhe aditivë për vajrat lubrifikues.
Mikhail Levitsky
Përfaqësuesit më të rëndësishëm të estereve janë yndyrnat.
Yndyrna, vajra
Yndyrnat- këto janë estere të glicerinës dhe monoatomike më të larta. Emri i përgjithshëm i komponimeve të tilla është trigliceride ose triacilglicerole, ku acil është një mbetje e acidit karboksilik -C(O)R. Përbërja e triglicerideve natyrore përfshin mbetje të acideve të ngopura (palmitik C 15 H 31 COOH, stearik C 17 H 35 COOH) dhe të pangopur (oleik C 17 H 33 COOH, linoleik C 17 H 31 COOH). Acidet më të larta karboksilike që janë pjesë e yndyrave kanë gjithmonë një numër çift atomesh karboni (C 8 - C 18) dhe një mbetje hidrokarbure të padegëzuar. Yndyrnat dhe vajrat natyrale janë përzierje të glicerideve të acideve karboksilike më të larta.
Përbërja dhe struktura e yndyrave mund të pasqyrohet nga formula e përgjithshme:

Esterifikimi- reagimi i formimit të estereve.

Përbërja e yndyrave mund të përfshijë mbetje të acideve karboksilike të ngopura dhe të pangopura në kombinime të ndryshme.
Në kushte normale, yndyrnat që përmbajnë mbetje të acideve të pangopura janë më shpesh të lëngshme. Ata quhen vajra. Në thelb, këto janë yndyrna me origjinë bimore - fara liri, kërpi, luledielli dhe vajra të tjerë (me përjashtim të vajrave të palmës dhe kokosit - të ngurta në kushte normale). Më pak të zakonshme janë yndyrat e lëngshme me origjinë shtazore, si vaji i peshkut. Shumica e yndyrnave natyrore me origjinë shtazore në kushte normale janë substanca të ngurta (me shkrirje të ulët) dhe përmbajnë kryesisht mbetje të acideve karboksilike të ngopura, për shembull, yndyrën e qengjit.
Përbërja e yndyrave përcakton vetitë e tyre fizike dhe kimike.
Vetitë fizike të yndyrave
Yndyrnat janë të patretshme në ujë, nuk kanë një pikë shkrirjeje të qartë dhe rriten ndjeshëm në vëllim kur shkrihen.
Gjendja agregate e yndyrave është e ngurtë, kjo për faktin se yndyrat përmbajnë mbetje të acideve të ngopura dhe molekulat e yndyrës janë të afta për paketim të dendur. Përbërja e vajrave përfshin mbetje të acideve të pangopura në konfigurimin cis, prandaj paketimi i dendur i molekulave është i pamundur, dhe gjendja e grumbullimit është e lëngshme.
Vetitë kimike të yndyrave
Yndyrnat (vajrat) janë estere dhe karakterizohen nga reaksione esterike.
Është e qartë se për yndyrnat që përmbajnë mbetje të acideve karboksilike të pangopura, të gjitha reaksionet e përbërjeve të pangopura janë karakteristike. Ato çngjyrosin ujin me brom dhe hyjnë në reaksione të tjera shtimi. Reagimi më i rëndësishëm në aspektin praktik është hidrogjenizimi i yndyrave. Esteret e ngurta fitohen nga hidrogjenizimi i yndyrave të lëngshme. Është ky reagim që qëndron në themel të prodhimit të margarinës - një yndyrë e fortë nga vajrat bimore. Në mënyrë konvencionale, ky proces mund të përshkruhet nga ekuacioni i reagimit:

Të gjitha yndyrnat, si esteret e tjerë, i nënshtrohen hidrolizës:

Hidroliza e estereve është një reaksion i kthyeshëm. Për të siguruar formimin e produkteve të hidrolizës, ajo kryhet në një mjedis alkalik (në prani të alkaleve ose Na 2 CO 3). Në këto kushte, hidroliza e yndyrave ndodh në mënyrë të kthyeshme dhe çon në formimin e kripërave të acideve karboksilike, të cilat quhen. yndyrnat në një mjedis alkalik quhen saponifikimin e yndyrave.
Kur yndyrat sapunohen, formohen glicerina dhe sapunët - kripërat e natriumit dhe kaliumit të acideve më të larta karboksilike:
Saponifikimi– hidroliza alkaline e yndyrave, prodhimi i sapunit.

Sapun– përzierjet e kripërave të natriumit (kaliumit) të acideve karboksilike të ngopura më të larta (sapun natriumi - i ngurtë, sapun kaliumi - i lëngshëm).
Sapunët janë surfaktantë (shkurtuar si surfaktantë, detergjentë). Efekti detergjent i sapunit është për faktin se sapuni emulsifikon yndyrnat. Sapunët formojnë micela me ndotës (relativisht, këto janë yndyrna me përfshirje të ndryshme).
Pjesa lipofile e molekulës së sapunit tretet në ndotës dhe pjesa hidrofile përfundon në sipërfaqen e micelës. Micelat ngarkohen në të njëjtën mënyrë, prandaj ato zmbrapsen, dhe ndotësi dhe uji shndërrohen në një emulsion (praktikisht, është ujë i ndotur).

Sapuni gjendet edhe në ujë, i cili krijon një mjedis alkalik.
Sapunët nuk mund të përdoren në ujë të fortë ose të detit, pasi stearatet e kalciumit (magnezit) që rezultojnë janë të patretshëm në ujë.

Nëse acidi fillestar është polibazik, atëherë formimi i ose estereve të plota zëvendësohen të gjitha grupet HO, ose zëvendësimi i pjesshëm i estereve acid është i mundur. Për acidet monobazike janë të mundshme vetëm esteret e plota (Fig. 1).
Oriz. 1. SHEMBUJ ESTERësh me bazë acidin inorganik dhe karboksilik
Nomenklatura e estereve. Emri krijohet si më poshtë: së pari tregohet grupi R , i bashkangjitur acidit, pastaj emri i acidit me prapashtesën “at” (si në emrat e kripërave inorganike: karbon në natriumi, nitrat në krom). Shembuj në Fig.2
Nëse përdorni të parëndësishme ( cm. EMRAT TRIVIAL TË SUBSTANCAVE) është emri i acidit fillestar, atëherë emri i përbërjes përfshin fjalën "ester", për shembull, C 3 H 7 COOC 5 H 11 amil ester i acidit butirik.
Klasifikimi dhe përbërja e estereve. Ndër esterët e studiuar dhe të përdorur gjerësisht, shumica janë komponime që rrjedhin nga acidet karboksilike. Esteret e bazuara në acide minerale (inorganike) nuk janë aq të ndryshme, sepse klasa e acideve minerale është më pak e madhe se acidet karboksilike (larmia e përbërjeve është një nga tiparet dalluese kimia organike).Kur numri i atomeve C në acidin karboksilik origjinal dhe alkoolin nuk i kalon 68, esterët përkatës janë lëngje vajore pa ngjyrë, më së shpeshti me erë frutash. Ata formojnë një grup esterësh frutash. Nëse një alkool aromatik (që përmban një bërthamë aromatike) është i përfshirë në formimin e një esteri, atëherë komponime të tilla, si rregull, kanë një erë lulesh dhe jo frutash. Të gjitha komponimet në këtë grup janë praktikisht të patretshme në ujë, por lehtësisht të tretshëm në shumicën e tretësve organikë. Këto komponime janë interesante për shkak të gamës së tyre të gjerë të aromave të këndshme (Tabela 1); disa prej tyre fillimisht u izoluan nga bimët dhe më vonë u sintetizuan artificialisht.
| Tabela 1. DISA ESTRE, me një aromë frutash ose lulesh (fragmentet e alkooleve origjinale në formulën e përbërjes dhe në emër janë të theksuara me shkronja të zeza) | ||
| Formula e Esterit | Emri | Aroma |
| CH 3 COO C 4 H 9 | Butil acetat | dardhë |
| C 3 H 7 COO CH 3 | Metil Ester i acidit butirik | mollë |
| C 3 H 7 COO C 2 H 5 | Etil Ester i acidit butirik | ananasi |
| C 4 H 9 COO C 2 H 5 | Etil | i kuq |
| C 4 H 9 COO C 5 H 11 | Isoamili ester i acidit izovalerik | banane |
| CH 3 COO CH 2 C 6 H 5 | Benzil acetat | jasemini |
| C 6 H 5 COO CH 2 C 6 H 5 | Benzil benzoat | me lule |
Grupi i tretë janë yndyrnat. Ndryshe nga dy grupet e mëparshme me bazë alkoolet monohidrike
ROH , të gjitha yndyrnat janë estere të alkoolit glicerol HOCH 2 CH(OH)CH 2 OH. Acidet karboksilike që përbëjnë yndyrnat, si rregull, kanë një zinxhir hidrokarburesh me 919 atome karboni. Yndyrna shtazore (gjalpë lope, qengji, sallo) plastikë, substanca të shkrirë. Yndyrna bimore (ulliri, fara pambuku, vaj luledielli) lëngje viskoze. Yndyrnat shtazore kryesisht përbëhen nga një përzierje e glicerideve të acidit stearik dhe palmitik (Fig. 3A, B). Vajrat vegjetale përmbajnë gliceride acidesh me një gjatësi zinxhiri karboni pak më të shkurtër: laurik C 11 H 23 COOH dhe miristik C 13 H 27 COOH. (si stearik dhe palmitik këto janë acide të ngopura). Vajra të tillë mund të ruhen në ajër për një kohë të gjatë pa ndryshuar konsistencën e tyre, dhe për këtë arsye quhen jo-tharëse. Në të kundërt, vaji i farave të lirit përmban glicerid të pangopur të acidit linoleik (Figura 3B). Kur aplikohet në një shtresë të hollë në sipërfaqe, vaji i tillë thahet nën ndikimin e oksigjenit atmosferik gjatë polimerizimit përgjatë lidhjeve të dyfishta dhe formohet një film elastik që është i pazgjidhshëm në ujë dhe tretës organikë. Vaji natyral i tharjes është bërë nga vaji i lirit.
Oriz. 3. GLICERIDET E ACIDEVE stearik dhe palmitik (A DHE B) përbërësit e yndyrës shtazore. Përbërësi i gliceridit të acidit linoleik (B) i vajit të lirit.
Estere të acideve minerale (alkil sulfate, alkil borate që përmbajnë fragmente të alkooleve më të ulëta C 18) lëngje vajore, estere të alkooleve më të larta (duke filluar nga C 9) përbërje të ngurta.
Vetitë kimike të estereve. Më karakteristikë e estereve të acideve karboksilike është ndarja hidrolitike (nën ndikimin e ujit) e lidhjes esterike; në një mjedis neutral ajo vazhdon ngadalë dhe përshpejtohet dukshëm në prani të acideve ose bazave, sepse Jonet H + dhe HO e katalizojnë këtë proces (Fig. 4A), me jonet hidroksil që veprojnë në mënyrë më efikase. Hidroliza në prani të alkaleve quhet saponifikimi. Nëse merrni një sasi alkali të mjaftueshme për të neutralizuar të gjithë acidin e formuar, atëherë ndodh saponifikimi i plotë i esterit. Ky proces kryhet në shkallë industriale dhe glicerina dhe acidet karboksilike më të larta (C 1519) fitohen në formën e kripërave të metaleve alkali, të cilat janë sapuni (Fig. 4B). Fragmentet e acideve të pangopura që përmbahen në vajrat bimore, si çdo përbërje e pangopur, mund të hidrogjenizohen, hidrogjeni ngjitet në lidhje të dyfishta dhe formohen përbërje të ngjashme me yndyrat shtazore (Fig. 4B). Duke përdorur këtë metodë, yndyrat e ngurta prodhohen industrialisht me bazë vaji të lulediellit, sojës ose misrit. Margarina është bërë nga produktet e hidrogjenizimit të vajrave bimore të përziera me yndyrna natyrore shtazore dhe aditivë të ndryshëm ushqimorë.Metoda kryesore e sintezës është ndërveprimi i një acidi karboksilik dhe një alkooli, i katalizuar nga acidi dhe i shoqëruar me lëshimin e ujit. Ky reagim është i kundërt me atë të treguar në Fig. 3A. Në mënyrë që procesi të vazhdojë në drejtimin e dëshiruar (sinteza e esterit), uji distilohet (distilohet) nga përzierja e reaksionit. Nëpërmjet studimeve speciale duke përdorur atome të etiketuara, u arrit të vërtetohej se gjatë procesit të sintezës, atomi O, i cili është pjesë e ujit që rezulton, shkëputet nga acidi (i shënuar me një kornizë me pika të kuqe), dhe jo nga alkooli ( opsioni i parealizuar theksohet me një kornizë blu me pika).
Duke përdorur të njëjtën skemë, fitohen esteret e acideve inorganike, për shembull, nitroglicerina (Fig. 5B). Në vend të acideve, mund të përdoren kloruret acide; metoda është e zbatueshme si për acidet karboksilike (Fig. 5C) dhe ato inorganike (Fig. 5D).
Ndërveprimi i kripërave të acidit karboksilik me halogjenët alkil
RCl gjithashtu çon në estere (Fig. 5D), reaksioni është i përshtatshëm në atë që është i pakthyeshëm; kripa inorganike e lëshuar hiqet menjëherë nga mjedisi i reaksionit organik në formën e një precipitati.Përdorimi i estereve. Formati etilik HCOOC 2 H 5 dhe acetati etilik H 3 COOC 2 H 5 përdoren si tretës për llaqet e celulozës (në bazë të nitrocelulozës dhe acetatit të celulozës).Esteret e bazuara në alkoole dhe acide më të ulëta (Tabela 1) përdoren në industrinë ushqimore për të krijuar esenca frutash, dhe esteret me bazë alkoolet aromatike në industrinë e parfumeve.
Lubrifikuesit, lubrifikantët, kompozimet ngopëse për letër (letër dylli) dhe lëkurë janë bërë nga dylli; ato përfshihen gjithashtu në kremrat kozmetikë dhe pomadat medicinale.
Yndyrnat, së bashku me karbohidratet dhe proteinat, përbëjnë një grup ushqimesh të nevojshme për të ushqyer; ato janë pjesë e të gjitha qelizave bimore dhe shtazore; përveç kësaj, kur grumbullohen në trup, ato luajnë rolin e një rezerve energjie. Për shkak të përçueshmërisë së ulët termike, shtresa e yndyrës mbron mirë kafshët (veçanërisht balenat e detit ose detet) nga hipotermia.
Yndyrnat shtazore dhe bimore janë lëndë të para për prodhimin e acideve karboksilike më të larta, detergjentëve dhe glicerinës (Fig. 4), të përdorura në industrinë kozmetike dhe si përbërës të lubrifikantëve të ndryshëm.
Nitroglicerina (Fig. 4) është një ilaç dhe eksploziv i njohur, baza e dinamitit.
Vajrat tharëse bëhen nga vajra bimore (Fig. 3), të cilat përbëjnë bazën e bojrave të vajit.
Esteret e acidit sulfurik (Fig. 2) përdoren në sintezën organike si reagentë alkilues (duke futur një grup alkil në një përbërje), dhe esteret e acidit fosforik (Fig. 5) përdoren si insekticide, si dhe aditivë për vajrat lubrifikues.
Mikhail Levitsky
LITERATURA Kartsova A.A. Pushtimi i materies. Kimi organike. Shtëpia Botuese Khimizdat, 1999Pustovalova L.M. Kimi organike. Phoenix, 2003
Esteret përmbajnë grupin funksional:
ku R dhe R" janë radikale të njëjta ose të ndryshme.
Esteret mund të konsiderohen gjithashtu si derivate të acideve në të cilat atomi i hidrogjenit në grupin karboksil zëvendësohet nga një radikal hidrokarbur (R"):
Vetitë fizike
Esteret e acideve më të ulëta karboksilike dhe alkooleve janë lëngje të paqëndrueshme, të patretshme në ujë. Shumë prej tyre kanë një erë të këndshme. Për shembull, butil butirati ka erë ananasi, izoamil acetati ka erë dardhe, etj.
Esteret e acideve yndyrore dhe alkooleve më të larta janë substanca dylli, pa erë dhe të patretshme në ujë. Aroma e këndshme e luleve dhe manave është kryesisht për shkak të pranisë së disa estereve në to.
Yndyrnat janë të shpërndara gjerësisht në natyrë. Së bashku me hidrokarburet dhe proteinat, ato janë pjesë e të gjithë organizmave bimorë dhe shtazorë dhe përbëjnë një nga pjesët kryesore të ushqimit tonë.
Sipas gjendjes së tyre të grumbullimit në temperaturën e dhomës, yndyrat ndahen në të lëngshme dhe të ngurta. Yndyrnat e ngurta, si rregull, formohen nga acidet e ngopura, ndërsa yndyrat e lëngshme (shpesh quhen vajra) formohen nga acidet e pangopura. Yndyrnat janë të tretshme në tretës organikë dhe të patretshëm në ujë.
Metodat themelore për marrjen e estereve:
Esterifikimi - ndërveprimi i acideve karboksilike dhe alkooleve, për shembull, prodhimi i acetatit etilik nga acidi acetik dhe alkooli etilik:
CH 3 COOH + C 2 H 5 OH = CH 3 COOC 2 H 5 + H 2 O
Vetitë kimike
1. Reaksion hidrolize ose saponifikimi.
Siç u përmend më lart, reaksioni i esterifikimit është i kthyeshëm, prandaj, në prani të acideve, do të ndodhë një reaksion i kundërt i quajtur hidrolizë, duke rezultuar në formimin e acideve yndyrore origjinale dhe alkoolit:
Reaksioni i hidrolizës katalizohet gjithashtu nga alkalet; Në këtë rast, hidroliza është e pakthyeshme:
meqenëse acidi karboksilik që rezulton formon një kripë me një alkali:
CH 3 – COOH + NaOH → CH 3 – COONa + H 2 O
2. Reaksioni i shtimit.
Esteret që përmbajnë një acid të pangopur ose alkool janë të aftë për reaksione shtesë. Për shembull, gjatë hidrogjenizimit katalitik ata shtojnë hidrogjen.
3. Reagimi i rikuperimit.
Reduktimi i estereve me hidrogjen rezulton në formimin e dy alkooleve:
4. Reagimi i formimit të amideve.
Nën ndikimin e amoniakut, esteret shndërrohen në amide acide dhe alkoole:
CH 3 -CO-O C 2 H 5 + NH 3 → CH 3 -CO-NH 2 + C 2 H 5 OH.
56) Yndyrna- këto janë përzierje esteresh të formuara nga glicerina e alkoolit trihidrik dhe acidet yndyrore më të larta. Formula e përgjithshme e yndyrave, ku R është radikalet e acideve yndyrore më të larta:
Më shpesh, përbërja e yndyrave përfshin acide të ngopura: acid palmitik C 15 H 31 COOH dhe acid stearik C 17 H 35 COOH, dhe acide të pangopura: acid oleik C 17 H 33 COOH dhe acid linoleik C 17 H 31 COOH.
Emri i përgjithshëm për përbërjet e acideve karboksilike me glicerinë është trigliceride.
Hidroliza e yndyrave në teknologji (saponifikimi i yndyrave). Yndyrnat kanë një rëndësi të madhe teknike: ato shërbejnë si materiale të nevojshme për prodhimin e sapunit dhe glicerinës. Sapunët janë kripëra të acideve yndyrore më të larta, tretësirat e të cilave kanë një efekt pastrues. Më të përhapurit janë sapunët me natrium, që përdoren në teknologji dhe në jetën e përditshme si detergjentë. Thelbi i prodhimit të sapunit është saponifikimi i yndyrave me një zgjidhje të hidroksidit të natriumit kur nxehet. Në këtë rast, yndyrnat ndahen në glicerinë dhe sapun.
Hidroliza, ose saponifikimi i yndyrave ndodh nën ndikimin e ujit (i kthyeshëm) ose alkaleve (i pakthyeshëm):
Pra: sapunët janë kripëra të acideve karboksilike më të larta. Sapunët konvencionalë përbëhen kryesisht nga një përzierje e kripërave të acideve palmitike, stearik dhe oleik. Kripërat e natriumit formojnë sapunë të ngurtë, kripërat e kaliumit formojnë sapunë të lëngshëm.
Për të ndarë përzierjen që rezulton të glicerinës dhe sapunit, shtohet një zgjidhje ujore e klorurit të natriumit, në të cilën, si në një elektrolit me të njëjtin jon natriumi, sapuni tretet shumë dobët. Si rezultat, ndodh delamination: në krye është një shtresë e zgjidhjes së sapunit, dhe më poshtë është një zgjidhje e glicerinës dhe klorurit të natriumit. Tretësira e sapunit derdhet në kallëpe ku ngurtësohet. Një tretësirë ujore e glicerinës avullohet, ndahet nga kloruri i natriumit dhe pastrohet me distilim.
Për prodhimin e sapunit përdoren yndyrna të ndryshme: sallo, gjalpë etj. Aktualisht për prodhimin e sapunit përdoren lëndë të para jo ushqimore. Acidet e nevojshme për këtë prodhohen në shkallë industriale duke oksiduar hidrokarburet që përbëjnë parafinën.
Vetitë kimike
1. Hidroliza në një mjedis acid
Aplikimi i yndyrave
Yndyrnat përdoren për ushqim. Disa vajra përdoren për të bërë kozmetikë (kremra, maska, pomada).
Një sërë yndyrash kanë vlerë medicinale: vaji i ricinit, vaji i gjembave të detit, vaji i peshkut, yndyra e patës.
Vajrat nga peshku i harengës dhe vaji i fokave përdoren për të ushqyer kafshët e fermës.
Vajrat vegjetale për tharje përdoren për prodhimin e vajrave tharëse.
Lëndët e para për prodhimin e margarinës janë shumë vajra bimore dhe vaj balene.
Yndyrnat shtazore përdoren për të prodhuar qirinj sapuni dhe stearin.
Yndyrnat përdoren për të prodhuar glicerinë dhe lubrifikantë.
1) Esteret – _________________________________________________________________.
Esteret – __________________________________________________________________
__________________________________________________________________________________
__________________________________________________________________________________:
Ku R dhe R / - _________________________________, e cila mund të jetë ose e njëjtë ose e ndryshme.
Grupi funksional i estereve quhet _________________________:
Përbërja molekulare e estereve shprehet me formulën e përgjithshme C-H-O-.
2) Etil ester i acidit acetik si përfaqësues i estereve.
3) Nomenklatura dhe izomeria e estereve
* Kur emërtohet esteret, sipas rregullave të nomenklaturës zëvendësuese IUPAC, fillimisht tregojnë emrin e grupit alkil të alkoolit, e më pas emrin e mbetjes së acidit, duke zëvendësuar prapashtesën –ova në emër të acidit me prapashtesën –tërshërë.
Etanoat etilik
2- mbetje grupi 1-alkil
alkool acid
* Izomerizmi strukturor
Brenda izomerisë së zinxhirit të klasës:
Izomerët e mëposhtëm korrespondojnë me formulën molekulare C 4 H 8 O 2:
Etil etanoat Propil metanoat Metil propanoat
Izomerizmi ndërklasor:
Etil etanoat Acidi butanoik
4) Hidroliza e estereve
o Acid:
H 2 O + CH 3 -CH 2 -OH
_______________ _____________ ________
o Alkaline:
NaOH + CH 3 -CH 2 -OH
______________ ______________ _________ ______________
5) Esteret në natyrë.
Shumë estere gjenden natyrshëm në lëngun e qelizave të luleve dhe frutave të bimëve.
Yndyrnat.
1) Përbërja dhe struktura e triglicerideve.
Yndyrna - ____________________________________________________________________________.
Përbërësit kryesorë të yndyrave janë _________________ –_____________________
____________________________________________________________________________________.
Skema që pasqyron strukturën e përgjithshme të triglicerideve:
Ku R 1, R 2, R 3 janë mbetje të acidit karboksilik (____________ CH 3 CH 2 CH 2 COOH, ________________ C 15 H 31 COOH, _____________ C 17 H 35 COOH, ________________ C 17 H 3 , ______________________ C 17 H 29 COOH.
2) Vetitë fizike.
3) Yndyrnat si lëndë ushqyese.
Yndyrnat janë një pjesë e rëndësishme e ushqimit të njerëzve dhe kafshëve. Në trup, gjatë procesit të hidrolizës, yndyrat zbërthehen në glicerinë dhe acide karboksilike më të larta. Më pas, brenda qelizave, yndyrat specifike për një organizëm të caktuar sintetizohen nga produktet e hidrolizës.
Yndyrnat janë burimi më i rëndësishëm i energjisë: oksidimi i tyre prodhon dy herë më shumë energji sesa oksidimi i karbohidrateve.
Detyrë shtëpie: §§39-40, 42.
1. Krijo ekuacione reaksioni që mund të përdoren për të kryer transformimet e mëposhtme: C 2 H 6 ® C 2 H 6 ® C 2 H 5 OH ® CH 3 COOH ® CH 3 COO C 2 H 5
2. Krijoni formulat strukturore të të gjithë izomerëve të mundshëm të përbërjes C 5 H 10 O 2 dhe emërtoni sipas rregullave të nomenklaturës zëvendësuese IUPAC.
Leksione 20, 21 Hidrokarburet: alkane, alkene, alkene, arene.
| Emrat e serive homologe Karakteristikat | Alkanet | Alkenet | Alkinet | Arena | ||
| 1. Përkufizimi | Hidrokarburet e ngopura aciklike, në molekulat e të cilave atomet e karbonit janë të lidhur me njëri-tjetrin vetëm me lidhje të vetme (të thjeshta) | Hidrokarburet aciklike të pangopura, në molekulat e të cilave 2 atome karboni janë të lidhur me një lidhje të dyfishtë | Hidrokarburet aciklike të pangopura, në molekulat e të cilave 2 atome karboni janë të lidhura me një lidhje të trefishtë | Hidrokarbure ciklike të pangopura, molekulat e të cilave përmbajnë një ose më shumë unaza benzeni | ||
| 2. Formula e përgjithshme | C n H 2n+2 | CnH2n | CnH2n-2 | CnH2n-6 | ||
| 3. Përfaqësuesi më i thjeshtë | metani | etenit | etin | benzenit | ||
| a) Formula molekulare | CH 4 | C2H4 | C2H2 | C6H6 | ||
| b) Formula strukturore | H ½ H¾C¾H ½ H | H H\/C═C/\H H | H¾CºC¾H | |||
| c) Formula elektronike | ||||||
| 4. Struktura hapësinore e molekulës: a) Forma | Metan - tetraedral Homologët e metanit, duke filluar me butan - zigzag | Në rajonin e lidhjes së dyfishtë - e sheshtë | Në zonën e lidhjes së trefishtë - cilindrike (lineare) | E sheshtë | ||
| b) Këndi i lidhjes | ||||||
| c) Natyra e lidhjes | beqare | dyfishtë | trefishtë | Aromatike | ||
| d) Gjatësia e lidhjes | 0,154 nm | 0,133 nm | 0,120 nm | 0,140 nm | ||
| 5. Mundësia e rrotullimit të atomeve të karbonit në raport me njëri-tjetrin në varësi të natyrës së lidhjes | Relativisht falas | Në lidhje me një lidhje të dyfishtë është e vështirë (e pamundur pa thyer lidhjen e dyfishtë) | Në lidhje me një lidhje të trefishtë është e vështirë (e pamundur pa thyer lidhjen e trefishtë) | Ndërmjet atomeve të karbonit të unazës së benzenit pengohet (e pamundur pa thyer unazën e benzenit) | ||
| 6. Emra të parëndësishëm | C 1 metan, C 2 etan, C 3 propan, C 4 butan (mbaresa –an, e klasifikuar si gjysmësistematike) | CH 2 = CH 2 etilen, CH 2 = CH – CH 3 propilen CH 2 = CH – CH 2 – CH 3 butilen | CHºCH acetilen | C 6 C 6 benzen | ||
| 7. Izomerizmi - | dukuria e ekzistencës së përbërjeve që kanë të njëjtën përbërje cilësore dhe sasiore, por strukturë kimike të ndryshme (rend i ndryshëm i lidhjes së atomeve në një molekulë); për hidrokarburet mund të jetë strukturor (zinxhirët; pozicionet e lidhjeve të shumta) dhe hapësinore. | |||||
| Strukturore | Izomerizmi i zinxhirit | CH 3 – CH 2 – CH 2 – CH 3 t vlim = - 0,5°C CH 3 – CH– CH 3 ï CH 3 t vlim = -1 0,2°C | CH 2 = CH – CH 2 – CH 3 buten-1 CH 2 = C – CH 3 ï CH 3 2-metilpropen | CHº– CH 2 –CH 2 – CH 3 pentine-1 CHºС – CH–– CH 3 ï CH 3 3-metilbugin-1 | - | |
| Izomerizmi i pozicionit të lidhjes së shumëfishtë | - | CH 2 =CH– CH 2 – CH 3 buten-1 CH 3 –CH= CH– CH 3 buten-2 | CHºС – CH 2 – CH 3 butine-1 CH 3 –Сº – CH 3 butine-2 | - | ||
| Izomerizmi hapësinor – cis-trans | - | Н 3 С Н\ ¤ С=С ¤ \ Н 3 С Н cis-izomer | H CH 3 \ ¤ C=C ¤ \ H 3 CH trans izomer | - | - | |
| Vetitë fizike | ||||||
| 1. Gjendja fizike: | C 1 -C 4 –_____, C 5 -C 15 – ________, C 16 – _______________________; | C 2 -C 4 –______, C 5 -C 17 –______, C 18 – ___________________; | C 2 -C 4 – _____, C 5 -C 16 –_______, C 17 – ___________________; | lëng (pa ngjyrë, shumë refraktiv, me erë karakteristike) | ||
| 2. t vlim. dhe t float. | me rritjen e M r, t bp rritet. dhe t float. | me rritjen e M r, t kip rritet | t kip. = 80,1°С, t shkrihet. =5,5°C | |||
| 3. tretshmëria në ujë | praktikisht i pazgjidhshëm | praktikisht i pazgjidhshëm | praktikisht i pazgjidhshëm | i pazgjidhshëm | ||
| 4. efekt fiziologjik në organizëm | - | - | - | përbërje shumë toksike | ||
| Vetitë kimike | ||||||
| Reaksionet e oksidimit: - oksidimi i plotë (djegia) - oksidimi jo i plotë | CH 4 +2O 2 →______+____+Q Përzierjet e metanit me oksigjen (1:2 për nga vëllimi) dhe ajrin (1:10) janë shpërthyese 2CH 4 +3O 2 → | C 2 H 4 +_O 2 → C 2 H 4 + (O) + H 2 O ® etilen glikol | _C 2 H 2 +_O 2 → | _C 6 H 6 +__O 2 → | ||
| Reaksionet e zëvendësimit (nën ndriçim me klor dhe brom) | 1) CH 4 +Cl 2 CH 3 -CH 3 + Cl 2 → 2) Gjatë halogjenimit të metanit, të gjithë atomet e hidrogjenit zëvendësohen në mënyrë të njëpasnjëshme dhe formohet një përzierje produktesh: CH 4 CH 3 Cl metan klorometan → CH 2 Cl 2 CHCl 3 diklorometan triklormetani ( kloro- → CCl 4 roform) tetraklorur karboni (tetraklorur karboni) Tretës, lëng i rëndë jo i ndezshëm - shuarje zjarri, i marrë nga klorifikimi i plotë i metanit: CH 4 +4Cl 2 3) ndërveprimet e tjera të plumbit formimi i përzierjes së izomerëve: CH 3 - CH 2 - CH 3 + 2Cl 2 → CH 3 ― CH 2 ― CH 2 Cl + + CH 3 ―CHCl— CH 3 + 2HCl | - | - | H +Br 2 halogjenimi H +HONO 2 ® nitrimi | ||
| Piroliza | C 2 H 6 CH 2 = CH 2 + H 2 | - | - | - | ||
| Izomerizimi | CH 3 – CH 2 – CH 2 – CH 3 ® | - | - | - | ||
| Reaksionet e shtimit: -halogjene | - | CH 2 = CH 2 + Br 2 ® çngjyrosje e ujit bromin (ose një zgjidhje bromi në tetrakloroetan) - një reagim cilësor ndaj hidrokarbureve me një lidhje të dyfishtë | СНºСН +Br 2 ® BrСН= СНBr +Br 2 ® | - | ||
| - hidrogjeni (hidrogjenizimi) | - | CH 2 = CH 2 + H 2 ® | СНºСН ________® | +3H 2 benzen cikloheksan | ||
| - ujë (hidratim) | - | CH 2 = CH 2 + H 2 O ® | CHºCH + H 2 O ® | - | ||
| - hidrokarburet e halogjenizuara | - | CH 2 = CH 2 + HCl ® | СНºСН + 2НCl ® | - | ||
| Reaksioni i polikrizimit (sinteza e BMC nga komponimet me peshë të ulët molekulare; NMC - monomer, BMC - polimer) | - | nCH 2 =CH 2 ® | trimerizimi 3 CHºCH | - | ||
Emrat e hidrokarbureve bazohen nënomenklatura sistematike e zëvendësimit janë parimet e pasqyruara në diagram:
|
|
|
Jo për UV
alkanet alkanet alkenet alkinet
2. Emri i hidrokarbureve të ngopura, të cilat merren si bazë për emrat e të gjitha përbërjeve të tjera organike ( rrënjët Numrat grekë janë të theksuar):
Tabela 1.
| Numri i atomeve C | Emri | Numri i atomeve C | Emri | Numri i atomeve C | Emri |
| C 1 | Meth sq | C 7 | Hept sq | Nga 13 | Tridek sq |
| C 2 | Kjo sq | Nga 8 | tetor sq | Nga 20 | Eikoza sq |
| C 3 | Prop sq | Nga 9 | Jo sq | Nga 21 | Gjenekoza sq |
| C 4 | Kabina sq | Nga 10 | dhjetor sq | Nga 22 | Dokoz sq |
| C 5 | I mbyllur sq | Nga 11 | Undek sq | Nga 30 | Triacontan |
| C 6 | Hex sq | Nga 12 | Dodek sq | Nga 40 | Tetrakontani |
Tabela 2.Emrat e numrave grekë
me të cilin tregohet
numri i zëvendësuesve identikë Tabela 3. Emrat e zëvendësve
| Numri i zëvendësuesve | Numri grek | Numri i zëvendësuesve | Numri grek | zv | Emri |
| 2 | di- | 7 | hepta- | CH 3 - | Cl- |
| 3 | tre- | 8 | tetë- | C 2 H 5 - | Br- |
| 4 | tetra- | 9 | jo- | C 3 H 7 - | une - |
| 5 | penta- | 10 | deka- | F- | NH 2 - |
| 6 | heksa- |
3) Sekuenca e veprimeve gjatë përpilimit të emrave të hidrokarbureve organike dhe derivateve të tyre.
A. Emrat e hidrokarbureve me varg të drejtë.
1. Emrat e alkaneve janë dhënë në tabelën 1.
2. Emrat e alkeneve dhe alkineve bazohen në emrat e alkaneve, në të cilët prapashtesa –ane zëvendësohet përkatësisht me prapashtesën –ene ose prapashtesën –ine. Në fund tregojmë pozicionin e lidhjes së shumëfishtë me një numër arab.
B. Emrat e hidrokarbureve me varg të degëzuar.
1. Gjeni qarkun kryesor:
2) Përfshin lidhjen e dyfishtë, të trefishtë,
3) Përfshin zëvendësues të tillë si F -, Cl -, Br -, I -.
2. Numërojmë nga fundi me të cilin është më afër
1) zv
2) Prioriteti i lidhjes së dyfishtë rritet
3) Lidhje e trefishtë nga lart poshtë
4) Sipas rendit alfabetik, ne tregojmë pozicionin e zëvendësuesve duke përdorur numra arabë (për emrat, shih Tabelën 3).
5) Ne i japim përparësi opsionit në të cilin shifra e parë e ndryshme është më e vogla.
6) Duke përdorur një parashtesë (shih tabelën 2) ne tregojmë numrin e zëvendësuesve identikë.
7) Shtoni emrin e zinxhirit kryesor në përputhje me numrin e atomeve të karbonit që përmbahen në të (shih rrënjët e theksuara në Tabelën 1)
8) Në rastin e alkeneve dhe alkineve, shtoni prapashtesën përkatëse –ene ose –ine në fund të emrit.
9) Ne tregojmë pozicionin e lidhjes së shumëfishtë me një numër arab (ne i japim përparësi opsionit në të cilin shifra është më e vogla).
C. Vendosni një vizë midis numrave dhe shkronjave dhe një presje midis numrave. Emri i hidrokarbureve aromatike bazohet në emrin e përfaqësuesit të tij më të thjeshtë, benzenit.