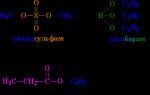Estera fizikālās īpašības. Nomenklatūra un izomerisms
Ja izejas skābe ir daudzbāziska, tad ir iespējama vai nu pilnu esteru veidošanās - tiek aizstātas visas HO grupas, vai arī skābes esteri - daļēja aizvietošana. Vienbāziskām skābēm iespējami tikai pilnie esteri (1. att.).
Rīsi. 1. ESTRU PIEMĒRI pamatojoties uz neorganisko un karbonskābi
Esteru nomenklatūra.
Nosaukums tiek izveidots šādi: vispirms norāda skābei piesaistīto grupu R, pēc tam skābes nosaukumu ar sufiksu “at” (kā neorganisko sāļu nosaukumos: ogleklis plkst nātrijs, nitrāts plkst hroms). Piemēri attēlā. 2

Rīsi. 2. ESTERU VĀRDI. Molekulu fragmenti un atbilstošie nosaukumu fragmenti ir izcelti vienā krāsā. Esteri parasti tiek uzskatīti par reakcijas produktiem starp skābi un spirtu; piemēram, butilpropionātu var uzskatīt par propionskābes un butanola reakcijas rezultātu.
Ja izmantojat triviālu ( cm. VIELU NOSAUKUMS) izejskābes nosaukums, tad savienojuma nosaukumā ir iekļauts vārds “esteris”, piemēram, C 3 H 7 COOC 5 H 11 - sviestskābes amilesteris.
Esteru klasifikācija un sastāvs.
Starp pētītajiem un plaši izmantotajiem esteriem lielākā daļa ir savienojumi, kas iegūti no karbonskābēm. Esteri, kuru pamatā ir minerālskābes (neorganiskās) skābes, nav tik daudzveidīgi, jo minerālskābju klasē ir mazāks skaits nekā karbonskābēm (savienojumu daudzveidība ir viena no organiskās ķīmijas pazīmēm).
Ja C atomu skaits sākotnējā karbonskābē un spirtā nepārsniedz 6–8, attiecīgie esteri ir bezkrāsaini eļļaini šķidrumi, visbiežāk ar augļu smaržu. Tie veido augļu esteru grupu. Ja estera veidošanā ir iesaistīts aromātiskais spirts (kas satur aromātisku kodolu), tad šādiem savienojumiem parasti ir ziedu, nevis augļu smarža. Visi šīs grupas savienojumi praktiski nešķīst ūdenī, bet viegli šķīst lielākajā daļā organisko šķīdinātāju. Šie savienojumi ir interesanti to plašā patīkamo aromātu klāsta dēļ (1. tabula), daži no tiem vispirms tika izolēti no augiem un vēlāk mākslīgi sintezēti.
| Tabula 1. DAŽI ESTERI, kam ir augļu vai ziedu aromāts (sākotnējo spirtu fragmenti savienojuma formulā un nosaukumā ir izcelti treknrakstā) | ||
| Estera formula | Vārds | Aromāts |
| CH 3 COO C 4 H 9 | Butils acetāts | bumbieris |
| C 3 H 7 COO CH 3 | Metil Sviestskābes esteris | ābolu |
| C 3 H 7 COO C2H5 | Etil Sviestskābes esteris | ananāsu |
| C 4 H 9 COO C2H5 | Etil | sārtināts |
| C 4 H 9 COO C5H11 | Isoamil izovalērskābes esteris | banāns |
| CH 3 COO CH 2 C 6 H 5 | Benzils acetāts | jasmīns |
| C 6 H 5 COO CH 2 C 6 H 5 | Benzils benzoāts | ziedu |
Palielinoties esteros iekļauto organisko grupu lielumam līdz C 15–30, savienojumi iegūst plastisku, viegli mīkstināmu vielu konsistenci. Šo grupu sauc par vaskiem; tie parasti ir bez smaržas. Bišu vasks satur dažādu esteru maisījumu, viena no vaska sastāvdaļām, kas tika izolēta un noteikta tā sastāva sastāvā, ir palmitīnskābes miricilesteris C 15 H 31 COOC 31 H 63. Ķīniešu vasks (košenīla ekskrēcijas produkts – Austrumāzijas kukaiņi) satur cerotīnskābes C 25 H 51 COOC 26 H 53 cerilesteri. Turklāt vaskos ir arī brīvās karbonskābes un spirti, kas ietver lielas organiskās grupas. Vaskus nesamitrina ūdens un tie šķīst benzīnā, hloroformā un benzolā.
Trešā grupa ir tauki. Atšķirībā no iepriekšējām divām grupām, kuru pamatā ir vienvērtīgie spirti ROH, visi tauki ir esteri, kas veidojas no trīsvērtīgā spirta glicerīna HOCH 2 – CH (OH) – CH 2 OH. Karbonskābēm, kas veido taukus, parasti ir ogļūdeņražu ķēde ar 9–19 oglekļa atomiem. Dzīvnieku tauki (govs sviests, jēra gaļa, speķis) ir plastmasas, kūstošas vielas. Augu tauki (olīvu, kokvilnas sēklu, saulespuķu eļļa) ir viskozi šķidrumi. Dzīvnieku tauki galvenokārt sastāv no stearīnskābes un palmitīnskābes glicerīdu maisījuma (3.A, B att.). Augu eļļas satur skābju glicerīdus ar nedaudz īsāku oglekļa ķēdes garumu: laurīnskābes C 11 H 23 COOH un miristskābes C 13 H 27 COOH. (tāpat kā stearīnskābe un palmitīnskābe, tās ir piesātinātās skābes). Šādas eļļas var ilgstoši uzglabāt gaisā, nemainot to konsistenci, un tāpēc tās sauc par nežāvējošām. Turpretim linsēklu eļļa satur nepiesātinātu linolskābes glicerīdu (3.B attēls). Uzklājot uz virsmas plānā kārtā, šāda eļļa atmosfēras skābekļa ietekmē izžūst polimerizācijas laikā pa dubultsaitēm, un veidojas elastīga plēve, kas nešķīst ūdenī un organiskajos šķīdinātājos. Dabiskā žāvēšanas eļļa ir izgatavota no linsēklu eļļas.

Rīsi. 3. STEARĪNSKĀBES UN PALMĪTSKĀBES GLICERĪDI (A UN B)– dzīvnieku tauku sastāvdaļas. Linolskābes glicerīds (B) ir linsēklu eļļas sastāvdaļa.
Minerālskābju esteri (alkilsulfāti, alkilborāti, kas satur zemāko spirtu C1-8 fragmentus) ir eļļaini šķidrumi, augstāko spirtu esteri (sākot no C9) ir cieti savienojumi.
Esteru ķīmiskās īpašības.
Karbonskābju esteriem raksturīgākā ir esteru saites hidrolītiskā (ūdens ietekmē) šķelšanās, kas neitrālā vidē notiek lēni un skābju vai bāzu klātbūtnē jūtami paātrinās, jo H + un HO – joni katalizē šo procesu (4.A att.), efektīvāk iedarbojoties hidroksiljoniem. Hidrolīzi sārmu klātbūtnē sauc par pārziepjošanu. Ja lietojat sārmu, kas ir pietiekams, lai neitralizētu visu izveidoto skābi, notiek pilnīga estera pārziepjošana. Šis process tiek veikts rūpnieciskā mērogā, un glicerīnu un augstākās karbonskābes (C 15–19) iegūst sārmu metālu sāļu veidā, kas ir ziepes (4.B att.). Nepiesātināto skābju fragmenti, kas atrodas augu eļļās, tāpat kā jebkuri nepiesātinātie savienojumi var tikt hidrogenēti, ūdeņradis pievienojas dubultsaitēm un veidojas dzīvnieku taukiem līdzīgi savienojumi (4.B att.). Izmantojot šo metodi, rūpnieciski tiek ražoti cietie tauki, kuru pamatā ir saulespuķu, sojas vai kukurūzas eļļa. Margarīnu ražo no augu eļļu hidrogenēšanas produktiem, kas sajaukti ar dabīgiem dzīvnieku taukiem un dažādām pārtikas piedevām.

Galvenā sintēzes metode ir karbonskābes un spirta mijiedarbība, ko katalizē skābe un ko papildina ūdens izdalīšanās. Šī reakcija ir pretēja tai, kas parādīta attēlā. 3A. Lai process noritētu vēlamajā virzienā (esteru sintēze), no reakcijas maisījuma tiek destilēts (destilēts) ūdens. Veicot īpašus pētījumus, izmantojot marķētos atomus, bija iespējams noskaidrot, ka sintēzes procesā O atoms, kas ir daļa no iegūtā ūdens, tiek atdalīts no skābes (atzīmēts ar sarkanu punktētu rāmi), nevis no spirta ( nerealizētā opcija ir izcelta ar zilu punktētu rāmi).
Izmantojot to pašu shēmu, tiek iegūti neorganisko skābju esteri, piemēram, nitroglicerīns (5.B att.). Skābju vietā var izmantot skābes hlorīdus, metode ir piemērojama gan karbonskābēm (5.C att.), gan neorganiskām skābēm (5.D att.).
Karbonskābes sāļu mijiedarbība ar RCl halogenīdiem arī noved pie esteru veidošanās (5.D att.), reakcija ir ērta ar to, ka tā ir neatgriezeniska - atbrīvotais neorganiskais sāls tiek nekavējoties izņemts no organiskās reakcijas vides nogulšņu veidā.
Esteru izmantošana.
Etilformiātu HCOOC 2 H 5 un etilacetātu H 3 COOC 2 H 5 izmanto kā šķīdinātājus celulozes lakām (uz nitrocelulozes un celulozes acetāta bāzes).
Esteri uz zemāko spirtu un skābju bāzes (1. tabula) tiek izmantoti pārtikas rūpniecībā, lai radītu augļu esences, bet esteri uz aromātisko spirtu bāzes smaržu rūpniecībā.
No vaskiem tiek izgatavoti pulēšanas līdzekļi, smērvielas, impregnējošie līdzekļi papīram (vaskotajam papīram) un ādai, tie ir iekļauti arī kosmētikas krēmos un ārstnieciskajās ziedēs.
Tauki kopā ar ogļhidrātiem un olbaltumvielām veido uzturam nepieciešamo pārtikas produktu kopumu, tie ir daļa no visām augu un dzīvnieku šūnām, turklāt, uzkrājoties organismā, tie spēlē enerģijas rezerves lomu. Zemās siltumvadītspējas dēļ tauku slānis labi aizsargā dzīvniekus (īpaši jūras dzīvniekus - vaļus vai valzirgus) no hipotermijas.
Dzīvnieku un augu tauki ir izejvielas augstāku karbonskābju, mazgāšanas līdzekļu un glicerīna ražošanai (4. att.), ko izmanto kosmētikas rūpniecībā un kā dažādu smērvielu sastāvdaļu.
Nitroglicerīns (4. att.) ir plaši pazīstama narkotika un sprāgstviela, dinamīta pamatā.
Žāvēšanas eļļas ir izgatavotas no augu eļļām (3. att.), kas veido eļļas krāsu pamatu.
Sērskābes esteri (2. att.) tiek izmantoti organiskajā sintēzē kā alkilēšanas (alkilgrupas ievadīšana savienojumā) reaģenti, bet fosforskābes esteri (5. att.) tiek izmantoti kā insekticīdi, kā arī kā piedevas smēreļļām.
Mihails Levitskis
Svarīgākie esteru pārstāvji ir tauki.
Tauki, eļļas
Tauki- tie ir glicerīna un augstākas vienatomu esteri. Šādu savienojumu vispārīgais nosaukums ir triglicerīdi vai triacilglicerīni, kur acils ir karbonskābes atlikums -C(O)R. Dabisko triglicerīdu sastāvā ietilpst piesātināto skābju (palmitīns C 15 H 31 COOH, stearīnskābe C 17 H 35 COOH) un nepiesātināto (oleīns C 17 H 33 COOH, linolskābe C 17 H 31 COOH) atlikumi. Augstākām karbonskābēm, kas ir tauku sastāvdaļa, vienmēr ir pāra oglekļa atomu skaits (C 8 - C 18) un nesazarots ogļūdeņraža atlikums. Dabiskie tauki un eļļas ir augstāko karbonskābju glicerīdu maisījumi.
Tauku sastāvu un struktūru var atspoguļot ar vispārīgo formulu:

Esterifikācija- esteru veidošanās reakcija.

Tauku sastāvā var būt gan piesātināto, gan nepiesātināto karbonskābju atliekas dažādās kombinācijās.
Normālos apstākļos tauki, kas satur nepiesātināto skābju atlikumus, visbiežāk ir šķidri. Tos sauc eļļas. Pamatā tie ir augu izcelsmes tauki – linsēklu, kaņepju, saulespuķu un citas eļļas (izņemot palmu un kokosriekstu eļļas – cietas normālos apstākļos). Retāk sastopami šķidrie dzīvnieku izcelsmes tauki, piemēram, zivju eļļa. Lielākā daļa dabisko dzīvnieku izcelsmes tauku normālos apstākļos ir cietas (zemas kušanas) vielas un satur galvenokārt piesātināto karbonskābju atlikumus, piemēram, jēra gaļas taukus.
Tauku sastāvs nosaka to fizikālās un ķīmiskās īpašības.
Tauku fizikālās īpašības
Tauki nešķīst ūdenī, tiem nav skaidras kušanas temperatūras un kausējot ievērojami palielinās tilpums.
Tauku agregātstāvoklis ir ciets, tas ir saistīts ar faktu, ka tauki satur piesātināto skābju atliekas un tauku molekulas spēj blīvi iesaiņot. Eļļu sastāvā ir nepiesātināto skābju atliekas cis konfigurācijā, tāpēc blīva molekulu iesaiņošana nav iespējama, un agregācijas stāvoklis ir šķidrs.
Tauku ķīmiskās īpašības
Tauki (eļļas) ir esteri, un tos raksturo esteru reakcijas.
Ir skaidrs, ka taukiem, kas satur nepiesātināto karbonskābju atlikumus, ir raksturīgas visas nepiesātināto savienojumu reakcijas. Tie atkrāso broma ūdeni un nonāk citās pievienošanās reakcijās. Praktiskā ziņā vissvarīgākā reakcija ir tauku hidrogenēšana. Cietos esterus iegūst, hidrogenējot šķidros taukus. Tieši šī reakcija ir pamatā margarīna ražošanai - cietiem taukiem no augu eļļām. Parasti šo procesu var aprakstīt ar reakcijas vienādojumu:

Visi tauki, tāpat kā citi esteri, tiek hidrolizēti:

Esteru hidrolīze ir atgriezeniska reakcija. Lai nodrošinātu hidrolīzes produktu veidošanos, to veic sārmainā vidē (sārmu vai Na 2 CO 3 klātbūtnē). Šādos apstākļos tauku hidrolīze notiek atgriezeniski un noved pie karbonskābju sāļu veidošanās, ko sauc. taukus sārmainā vidē sauc tauku pārziepjošana.
Kad tauki tiek pārziepjoti, veidojas glicerīns un ziepes - augstāko karbonskābju nātrija un kālija sāļi:
Pārziepjošana– tauku sārmaina hidrolīze, ziepju ražošana.

Ziepes– augstāk piesātināto karbonskābju nātrija (kālija) sāļu maisījumi (nātrija ziepes – cietas, kālija ziepes – šķidras).
Ziepes ir virsmaktīvās vielas (saīsināti kā virsmaktīvās vielas, mazgāšanas līdzekļi). Ziepju mazgāšanas efekts ir saistīts ar to, ka ziepes emulģē taukus. Ziepes veido micellas ar piesārņotājiem (nosacīti tie ir tauki ar dažādiem ieslēgumiem).
Ziepju molekulas lipofīlā daļa piesārņotājā izšķīst, un hidrofilā daļa nonāk uz micellas virsmas. Micellas tiek uzlādētas vienādi, tāpēc tās atgrūž, un piesārņotājs un ūdens pārvēršas emulsijā (praktiski tas ir netīrs ūdens).

Ziepes rodas arī ūdenī, kas rada sārmainu vidi.
Ziepes nevar lietot cietā un jūras ūdenī, jo iegūtie kalcija (magnija) stearāti ūdenī nešķīst.

Ja izejas skābe ir daudzbāziska, tad var veidoties vai nu pilnie esteri, visas HO grupas ir aizvietotas, vai arī iespējama skābes esteru daļēja aizvietošana. Vienbāziskām skābēm iespējami tikai pilnie esteri (1. att.).
Rīsi. 1. ESTRU PIEMĒRI pamatojoties uz neorganisko un karbonskābi
Esteru nomenklatūra. Nosaukums tiek izveidots šādi: vispirms tiek norādīta grupa R , kas pievienots skābei, tad skābes nosaukums ar sufiksu “at” (kā neorganisko sāļu nosaukumos: ogleklis plkst nātrijs, nitrāts plkst hroms). Piemēri attēlā.2
Ja izmantojat triviālu ( cm. TRIVIĀLI VIELU NOSAUKUMS) ir izejskābes nosaukums, tad savienojuma nosaukumā ir ietverts vārds “esteris”, piemēram, sviestskābes C 3 H 7 COOC 5 H 11 amilesteris.
Esteru klasifikācija un sastāvs. Starp pētītajiem un plaši izmantotajiem esteriem lielākā daļa ir savienojumi, kas iegūti no karbonskābēm. Esteri, kuru pamatā ir minerālskābes (neorganiskās) skābes, nav tik daudzveidīgi, jo minerālskābju klase ir mazāka nekā karbonskābēm (savienojumu daudzveidība ir viena no atšķirīgajām iezīmēm organiskā ķīmija).Ja C atomu skaits sākotnējā karbonskābē un spirtā nepārsniedz 68, attiecīgie esteri ir bezkrāsaini eļļaini šķidrumi, visbiežāk ar augļu smaržu. Tie veido augļu esteru grupu. Ja estera veidošanā ir iesaistīts aromātiskais spirts (kas satur aromātisku kodolu), tad šādiem savienojumiem parasti ir ziedu, nevis augļu smarža. Visi šīs grupas savienojumi praktiski nešķīst ūdenī, bet viegli šķīst lielākajā daļā organisko šķīdinātāju. Šie savienojumi ir interesanti to plašā patīkamo aromātu klāsta dēļ (1. tabula), daži no tiem vispirms tika izolēti no augiem un vēlāk mākslīgi sintezēti.
| Tabula 1. DAŽI ESTERI, kam ir augļu vai ziedu aromāts (sākotnējo spirtu fragmenti savienojuma formulā un nosaukumā ir izcelti treknrakstā) | ||
| Estera formula | Vārds | Aromāts |
| CH 3 COO C 4 H 9 | Butils acetāts | bumbieris |
| C 3 H 7 COO CH 3 | Metil Sviestskābes esteris | ābolu |
| C 3 H 7 COO C2H5 | Etil Sviestskābes esteris | ananāsu |
| C 4 H 9 COO C2H5 | Etil | sārtināts |
| C 4 H 9 COO C5H11 | Isoamil izovalērskābes esteris | banāns |
| CH 3 COO CH 2 C 6 H 5 | Benzils acetāts | jasmīns |
| C 6 H 5 COO CH 2 C 6 H 5 | Benzils benzoāts | ziedu |
Trešā grupa ir tauki. Atšķirībā no iepriekšējām divām grupām, kuru pamatā ir vienvērtīgie spirti
ROH , visi tauki ir glicerīna spirta HOCH 2 CH(OH)CH 2 OH esteri. Karbonskābēm, kas veido taukus, parasti ir ogļūdeņražu ķēde ar 919 oglekļa atomiem. Dzīvnieku tauki (govs sviests, jēra gaļa, speķis) plastmasa, kausējamas vielas. Augu tauki (olīvu, kokvilnas sēklu, saulespuķu eļļa) viskozi šķidrumi. Dzīvnieku tauki galvenokārt sastāv no stearīnskābes un palmitīnskābes glicerīdu maisījuma (3.A, B att.). Augu eļļas satur skābju glicerīdus ar nedaudz īsāku oglekļa ķēdes garumu: laurīnskābes C 11 H 23 COOH un miristskābes C 13 H 27 COOH. (tāpat kā stearīnskābe un palmitīnskābe, tās ir piesātinātās skābes). Šādas eļļas var ilgstoši uzglabāt gaisā, nemainot to konsistenci, un tāpēc tās sauc par nežāvējošām. Turpretim linsēklu eļļa satur nepiesātinātu linolskābes glicerīdu (3.B attēls). Uzklājot uz virsmas plānā kārtā, šāda eļļa atmosfēras skābekļa ietekmē izžūst polimerizācijas laikā pa dubultsaitēm, un veidojas elastīga plēve, kas nešķīst ūdenī un organiskajos šķīdinātājos. Dabiskā žāvēšanas eļļa ir izgatavota no linsēklu eļļas.
Rīsi. 3. STEARĪNSKĀBES UN PALMĪTSKĀBES GLICERĪDI (A UN B) dzīvnieku tauku sastāvdaļas. Linolskābes glicerīda (B) sastāvdaļa linsēklu eļļā.
Minerālskābju esteri (alkilsulfāti, alkilborāti, kas satur zemāko spirtu C 18 fragmentus) eļļaini šķidrumi, augstāko spirtu esteri (sākot no C 9) cietie savienojumi.
Esteru ķīmiskās īpašības. Karbonskābju esteriem raksturīgākā ir esteru saites hidrolītiskā (ūdens ietekmē) šķelšanās, kas neitrālā vidē notiek lēni un skābju vai bāzu klātbūtnē jūtami paātrinās, jo H + un HO joni katalizē šo procesu (4.A att.), un hidroksiljoni darbojas efektīvāk. Hidrolīzi sārmu klātbūtnē sauc par pārziepjošanu. Ja lietojat sārmu, kas ir pietiekams, lai neitralizētu visu izveidoto skābi, notiek pilnīga estera pārziepjošana. Šis process tiek veikts rūpnieciskā mērogā, un glicerīnu un augstākās karbonskābes (C 1519) iegūst sārmu metālu sāļu veidā, kas ir ziepes (4.B att.). Nepiesātināto skābju fragmenti, kas atrodas augu eļļās, tāpat kā jebkuri nepiesātinātie savienojumi var tikt hidrogenēti, ūdeņradis pievienojas dubultsaitēm un veidojas dzīvnieku taukiem līdzīgi savienojumi (4.B att.). Izmantojot šo metodi, rūpnieciski tiek ražoti cietie tauki, kuru pamatā ir saulespuķu, sojas vai kukurūzas eļļa. Margarīnu ražo no augu eļļu hidrogenēšanas produktiem, kas sajaukti ar dabīgiem dzīvnieku taukiem un dažādām pārtikas piedevām.Galvenā sintēzes metode ir karbonskābes un spirta mijiedarbība, ko katalizē skābe un ko papildina ūdens izdalīšanās. Šī reakcija ir pretēja tai, kas parādīta attēlā. 3A. Lai process noritētu vēlamajā virzienā (esteru sintēze), no reakcijas maisījuma tiek destilēts (destilēts) ūdens. Veicot īpašus pētījumus, izmantojot marķētos atomus, bija iespējams noskaidrot, ka sintēzes procesā O atoms, kas ir daļa no iegūtā ūdens, tiek atdalīts no skābes (atzīmēts ar sarkanu punktētu rāmi), nevis no spirta ( nerealizētā opcija ir izcelta ar zilu punktētu rāmi).
Izmantojot to pašu shēmu, tiek iegūti neorganisko skābju esteri, piemēram, nitroglicerīns (5.B att.). Skābju vietā var izmantot skābes hlorīdus, metode ir piemērojama gan karbonskābēm (5.C att.), gan neorganiskām skābēm (5.D att.).
Karbonskābes sāļu mijiedarbība ar alkilhalogenīdiem
RCl noved arī pie esteru veidošanās (5.D att.), reakcija ir ērta ar to, ka tā ir neatgriezeniska, izdalītais neorganiskais sāls tiek nekavējoties izņemts no organiskās reakcijas vides nogulšņu veidā.Esteru izmantošana. Etilformiātu HCOOC 2 H 5 un etilacetātu H 3 COOC 2 H 5 izmanto kā šķīdinātājus celulozes lakām (uz nitrocelulozes un celulozes acetāta bāzes).Esteri uz zemāko spirtu un skābju bāzes (1. tabula) tiek izmantoti pārtikas rūpniecībā, lai radītu augļu esences, bet esteri uz aromātisko spirtu bāzes smaržu rūpniecībā.
No vaskiem tiek izgatavoti pulēšanas līdzekļi, smērvielas, impregnējošie līdzekļi papīram (vaskotajam papīram) un ādai, tie ir iekļauti arī kosmētikas krēmos un ārstnieciskajās ziedēs.
Tauki kopā ar ogļhidrātiem un olbaltumvielām veido uzturam nepieciešamo pārtikas produktu kopumu, tie ir daļa no visām augu un dzīvnieku šūnām, turklāt, uzkrājoties organismā, tie spēlē enerģijas rezerves lomu. Zemās siltumvadītspējas dēļ tauku slānis labi pasargā dzīvniekus (īpaši jūras vaļus vai valzirgus) no hipotermijas.
Dzīvnieku un augu tauki ir izejvielas augstāku karbonskābju, mazgāšanas līdzekļu un glicerīna ražošanai (4. att.), ko izmanto kosmētikas rūpniecībā un kā dažādu smērvielu sastāvdaļu.
Nitroglicerīns (4. att.) ir plaši pazīstama narkotika un sprāgstviela, dinamīta pamatā.
Žāvēšanas eļļas ir izgatavotas no augu eļļām (3. att.), kas veido eļļas krāsu pamatu.
Sērskābes esteri (2. att.) tiek izmantoti organiskajā sintēzē kā alkilēšanas (alkilgrupas ievadīšana savienojumā) reaģenti, bet fosforskābes esteri (5. att.) tiek izmantoti kā insekticīdi, kā arī kā piedevas smēreļļām.
Mihails Levitskis
LITERATŪRA Kartsova A.A. Matērijas iekarošana. Organiskā ķīmija. Izdevniecība Khimizdat, 1999Pustovalova L.M. Organiskā ķīmija. Fēnikss, 2003
Esteri satur funkcionālo grupu:
kur R un R" ir vienādi vai atšķirīgi radikāļi.
Esterus var uzskatīt arī par skābju atvasinājumiem, kuros ūdeņraža atoms karboksilgrupā ir aizstāts ar ogļūdeņraža radikāli (R):
Fizikālās īpašības
Zemāko karbonskābju un spirtu esteri ir gaistoši, ūdenī nešķīstoši šķidrumi. Daudziem no tiem ir patīkama smarža. Piemēram, butilbutirāts smaržo pēc ananāsiem, izoamilacetāts pēc bumbieriem utt.
Augstāko taukskābju un spirtu esteri ir vaskveida vielas, bez smaržas un nešķīst ūdenī. Patīkamais ziedu un ogu aromāts lielā mērā ir saistīts ar noteiktu esteru klātbūtni tajos.
Tauki dabā ir plaši izplatīti. Kopā ar ogļūdeņražiem un olbaltumvielām tie ir daļa no visiem augu un dzīvnieku organismiem un ir viena no galvenajām mūsu pārtikas sastāvdaļām.
Saskaņā ar to agregācijas stāvokli istabas temperatūrā taukus iedala šķidros un cietos. Cietos taukus, kā likums, veido piesātinātās skābes, savukārt šķidros taukus (bieži sauc par eļļām) veido nepiesātinātās skābes. Tauki šķīst organiskajos šķīdinātājos un nešķīst ūdenī.
Pamatmetodes esteru iegūšanai:
Esterifikācija - karbonskābju un spirtu mijiedarbība, piemēram, etilacetāta ražošana no etiķskābes un etilspirta:
CH 3 COOH + C 2 H 5 OH = CH 3 COOC 2 H 5 + H 2 O
Ķīmiskās īpašības
1. Hidrolīzes vai pārziepjošanas reakcija.
Kā minēts iepriekš, esterifikācijas reakcija ir atgriezeniska, tāpēc skābju klātbūtnē notiks apgrieztā reakcija, ko sauc par hidrolīzi, kā rezultātā veidojas sākotnējās taukskābes un spirts:
Hidrolīzes reakciju katalizē arī sārmi; šajā gadījumā hidrolīze ir neatgriezeniska:
jo iegūtā karbonskābe veido sāli ar sārmu:
CH 3 – COOH + NaOH → CH 3 – COONa + H 2 O
2. Pievienošanas reakcija.
Esteri, kas satur nepiesātinātu skābi vai spirtu, spēj pievienoties reakcijas. Piemēram, katalītiskās hidrogenēšanas laikā tie pievieno ūdeņradi.
3. Atveseļošanās reakcija.
Esteru reducēšana ar ūdeņradi izraisa divu spirtu veidošanos:
4. Amīdu veidošanās reakcija.
Amonjaka ietekmē esteri tiek pārvērsti skābju amīdos un spirtos:
CH 3 -CO-O C 2 H 5 + NH 3 → CH 3 -CO-NH 2 + C 2 H 5 OH.
56) Tauki- tie ir esteru maisījumi, ko veido trīsvērtīgā spirta glicerīns un augstākas taukskābes. Vispārējā tauku formula, kur R ir augstāko taukskābju radikāļi:
Visbiežāk tauku sastāvā ir piesātinātās skābes: palmitīnskābe C 15 H 31 COOH un stearīnskābe C 17 H 35 COOH, un nepiesātinātās skābes: oleīnskābe C 17 H 33 COOH un linolskābe C 17 H 31 COOH.
Vispārējais nosaukums karbonskābju savienojumiem ar glicerīnu ir triglicerīdi.
Tauku hidrolīze tehnoloģijā (tauku pārziepjošana). Taukiem ir liela tehniskā nozīme: tie kalpo kā nepieciešamie materiāli ziepju un glicerīna ražošanai. Ziepes ir augstāko taukskābju sāļi, kuru šķīdumiem ir attīroša iedarbība. Visizplatītākās ir nātrija ziepes, ko izmanto tehnoloģijā un ikdienā kā mazgāšanas līdzekļus. Ziepju pagatavošanas būtība ir karsējot tauku pārziepjošana ar nātrija hidroksīda šķīdumu. Šajā gadījumā tauki tiek sadalīti glicerīnā un ziepēs.
Tauku hidrolīze jeb pārziepjošana notiek ūdens (atgriezeniska) vai sārmu (neatgriezeniska) ietekmē:
Tātad: ziepes ir augstāku karbonskābju sāļi. Parastās ziepes galvenokārt sastāv no palmitīnskābes, stearīnskābes un oleīnskābes sāļu maisījuma. Nātrija sāļi veido cietas ziepes, kālija sāļi veido šķidrās ziepes.
Lai atdalītu iegūto glicerīna un ziepju maisījumu, pievieno nātrija hlorīda ūdens šķīdumu, kurā, tāpat kā elektrolītā ar to pašu nātrija jonu, ziepes šķīst ļoti slikti. Tā rezultātā notiek atslāņošanās: augšpusē ir ziepju šķīduma slānis, un zemāk ir glicerīna un nātrija hlorīda šķīdums. Ziepju šķīdumu lej veidnēs, kur tas sacietē. Glicerīna ūdens šķīdumu iztvaicē, atdala no nātrija hlorīda un attīra ar destilāciju.
Ziepju gatavošanai tiek izmantoti dažādi tauki: speķis, sviests u.c. Šobrīd ziepju ražošanai tiek izmantotas nepārtikas izejvielas. Tam nepieciešamās skābes tiek ražotas rūpnieciskā mērogā, oksidējot ogļūdeņražus, kas veido parafīnu.
Ķīmiskās īpašības
1. Hidrolīze skābā vidē
Tauku pielietošana
Tauki tiek izmantoti pārtikā. Dažas eļļas tiek izmantotas kosmētikas (krēmu, masku, ziežu) pagatavošanai.
Vairākiem taukiem ir ārstnieciska vērtība: rīcineļļa, smiltsērkšķu eļļa, zivju eļļa, zosu tauki.
Lauksaimniecības dzīvnieku barošanai izmanto siļķu zivju eļļas un roņu eļļu.
Žāvēšanas eļļu ražošanai izmanto kaltējamās augu eļļas.
Margarīna ražošanas izejvielas ir daudzas augu eļļas un vaļu eļļa.
Dzīvnieku taukus izmanto ziepju un stearīna sveču ražošanā.
Tauki tiek izmantoti glicerīna un smērvielu ražošanai.
1) Esteri – ______________________________________________________________________.
Esteri – __________________________________________________________________
__________________________________________________________________________________
__________________________________________________________________________________:
Kur R un R / - _________________________________, kas var būt vienādi vai atšķirīgi.
Esteru funkcionālo grupu sauc par ______________________________:
Esteru molekulāro sastāvu izsaka ar vispārīgo formulu C-H-O-.
2) Etiķskābes etilesteris kā esteru pārstāvis.
3) Esteru nomenklatūra un izomērija
* Kad nosaukts esteri, saskaņā ar IUPAC aizvietojošās nomenklatūras noteikumiem, vispirms norāda spirta alkilgrupas nosaukumu, bet pēc tam skābes atlikuma nosaukumu, skābes nosaukumā aizstājot sufiksu –ova ar piedēkli –oat.
Etiletanolāts
2-atlikuma 1-alkilgrupa
skābs alkohols
* Strukturālā izomērija
Klases ietvaros – ķēdes izomērija:
Šādi izomēri atbilst molekulārajai formulai C 4 H 8 O 2:
Etiletanolāts Propilmetanoāts Metilpropanoāts
Starpklases izomerisms:
Etiletanolāts Butānskābe
4) Esteru hidrolīze
o skābs:
H2O + CH3-CH2-OH
_______________ _____________ ________
o Sārmains:
NaOH + CH3-CH2-OH
______________ ______________ _________ ______________
5) Esteri dabā.
Daudzi esteri dabiski atrodas augu ziedu un augļu šūnu sulā.
Tauki.
1) Triglicerīdu sastāvs un struktūra.
Tauki - ____________________________________________________________________________.
Galvenās tauku sastāvdaļas ir ____________________ –__________________________
____________________________________________________________________________________.
Shēma, kas atspoguļo triglicerīdu vispārējo struktūru:
Kur R1, R2, R3 ir karbonskābes atlikumi (____________ CH 3 CH 2 CH 2 COOH, ________________ C 15 H 31 COOH, _____________ C 17 H 35 COOH, ________________ C 17 H 33 COOH, ____ 7 , ____________________________ C 17 H 29 COOH.
2) Fizikālās īpašības.
3) Tauki kā barības vielas.
Tauki ir svarīga cilvēku un dzīvnieku pārtikas sastāvdaļa. Organismā hidrolīzes procesā tauki tiek sadalīti glicerīnā un augstākās karbonskābēs. Pēc tam šūnu iekšienē no hidrolīzes produktiem tiek sintezēti konkrētam organismam raksturīgie tauki.
Tauki ir vissvarīgākais enerģijas avots: to oksidēšanās rada divreiz vairāk enerģijas nekā ogļhidrātu oksidēšana.
Mājas darbs: §§39-40, 42.
1. Izveidojiet reakcijas vienādojumus, kurus var izmantot, lai veiktu šādas pārvērtības: C 2 H 6 ® C 2 H 6 ® C 2 H 5 OH ® CH 3 COOH ® CH 3 COO C 2 H 5
2. Sastādiet visu iespējamo sastāva C 5 H 10 O 2 izomēru strukturālās formulas un piešķiriet tiem nosaukumus saskaņā ar IUPAC aizstājējnomenklatūras noteikumiem.
Lekcijas 20, 21 Ogļūdeņraži: alkāni, alkēni, alkēni, arēni.
| Homoloģisko sēriju nosaukumi Raksturojums | Alkāni | Alkēni | Alkīni | Arēnas | ||
| 1. Definīcija | Acikliskie piesātinātie ogļūdeņraži, kuru molekulās oglekļa atomi ir saistīti viens ar otru tikai ar vienkāršām (vienkāršām) saitēm | Acikliskie nepiesātinātie ogļūdeņraži, kuru molekulās 2 oglekļa atomi ir savienoti ar dubultsaiti | Acikliskie nepiesātinātie ogļūdeņraži, kuru molekulās 2 oglekļa atomi ir saistīti ar trīskāršo saiti | cikliski nepiesātināti ogļūdeņraži, kuru molekulas satur vienu vai vairākus benzola gredzenus | ||
| 2. Vispārīgā formula | C n H 2n+2 | CnH2n | CnH2n-2 | CnH2n-6 | ||
| 3. Vienkāršākais pārstāvis | metāns | etēns | etīns | benzols | ||
| a) Molekulārā formula | CH 4 | C2H4 | C2H2 | C6H6 | ||
| b) Strukturālā formula | H ½ H¾C¾H ½ H | H H\/C═C/\H H | H¾CºC¾H | |||
| c) Elektroniskā formula | ||||||
| 4. Molekulas telpiskā uzbūve: a) Forma | Metāns - tetraedris Metāna homologi, sākot ar butānu - zigzags | Divkāršās saites reģionā - plakana | Trīskāršās saites zonā - cilindriska (lineāra) | Plakans | ||
| b) Savienojuma leņķis | ||||||
| c) Savienojuma veids | viens | dubultā | trīskāršs | Aromātisks | ||
| d) Saites garums | 0,154 nm | 0,133 nm | 0,120 nm | 0,140 nm | ||
| 5. Oglekļa atomu rotācijas iespēja vienam pret otru atkarībā no saites rakstura | Salīdzinoši bezmaksas | Kas attiecas uz dubultsaiti, tas ir grūti (neiespējams, nepārraujot dubultsaiti) | Attiecībā uz trīskāršo saiti tas ir sarežģīti (neiespējams, nepārraujot trīskāršo saiti) | Starp benzola gredzena oglekļa atomiem ir traucēta (neiespējami, nesalaužot benzola gredzenu) | ||
| 6. Triviālie nosaukumi | C 1 metāns, C 2 etāns, C 3 propāns, C 4 butāns (beidzas -an, klasificēts kā daļēji sistemātisks) | CH 2 = CH 2 etilēns, CH 2 = CH – CH 3 propilēns CH 2 = CH – CH 2 – CH 3 butilēns | CHºCH acetilēns | C 6 C 6 benzols | ||
| 7. Izomērisms – | tādu savienojumu esamības fenomens, kuriem ir vienāds kvalitatīvais un kvantitatīvais sastāvs, bet atšķirīga ķīmiskā struktūra (atšķirīga atomu savienojuma secība molekulā); ogļūdeņražiem tas var būt strukturāls (ķēdes; vairāku saišu pozīcijas) un telpisks. | |||||
| Strukturāls | Ķēdes izomerisms | CH 3 – CH 2 – CH 2 – CH 3 t vārīšanās temperatūra = - 0,5°C CH 3 – CH– CH 3 ï CH 3 t vārīšanās temperatūra = -1 0,2°C | CH 2 = CH – CH 2 – CH 3 butēns-1 CH 2 = C – CH 3 ï CH 3 2-metilpropēns | CHºС CH 2 –CH 2 – CH 3 pentīns-1 CHºС – CH–– CH 3 ï CH 3 3-metilbugin-1 | - | |
| Vairāku saišu pozīcijas izomērija | - | CH 2 =CH– CH 2 – CH 3 butēns-1 CH 3 –CH= CH– CH 3 butēns-2 | CHºС – CH 2 – CH 3 butīns-1 CH 3 –Сº С– CH 3 butīns-2 | - | ||
| Telpiskā – cis-trans izomērija | - | Н 3 С Н\ ¤ С=С ¤ \ Н 3 С Н cis-izomērs | H CH 3 \ ¤ C=C ¤ \ H 3 CH trans izomērs | - | - | |
| Fizikālās īpašības | ||||||
| 1. fiziskais stāvoklis: | C 1 - C 4 -_____, C 5 - C 15 - ________, C 16 - ____________________________; | C2-C4-______, C5-C17-______, C18-_______________________; | C 2 - C 4 - _____, C 5 - C 16 -_______, C 17 - _______________________; | šķidrums (bezkrāsains, ļoti refrakcijas, ar raksturīgu smaržu) | ||
| 2. t vāra. un t peldēt. | palielinoties M r, t bp palielinās. un t peldēt. | palielinoties M r, t kip palielinās | t kip. = 80,1°С, t izkausēt. =5,5°C | |||
| 3. šķīdība ūdenī | praktiski nešķīstošs | praktiski nešķīstošs | praktiski nešķīstošs | nešķīstošs | ||
| 4. fizioloģiskā ietekme uz ķermeni | - | - | - | ļoti toksisks savienojums | ||
| Ķīmiskās īpašības | ||||||
| Oksidācijas reakcijas: - pilnīga oksidēšanās (sadegšana) - nepilnīga oksidēšanās | CH 4 +2O 2 →______+____+Q Metāna maisījumi ar skābekli (1:2 pēc tilpuma) un gaisu (1:10) ir sprādzienbīstami 2CH 4 +3O 2 → | C 2 H 4 +_O 2 → C 2 H 4 + (O)+ H 2 O ® etilēnglikols | _C 2 H 2 +_O 2 → | _C 6 H 6 +__O 2 → | ||
| Aizvietošanas reakcijas (apgaismojumā ar hloru un bromu) | 1) CH 4 +Cl 2 CH 3 -CH 3 + Cl 2 → 2) Metāna halogenēšanas laikā tiek secīgi nomainīti visi ūdeņraža atomi un veidojas produktu maisījums: CH 4 CH 3 Cl metāns hlormetāns → CH 2 Cl 2 CHCl 3 dihlormetāns trihlormetāns ( chloro- → CCl 4 roform) tetrahlorogleklis (tetrahlorīds) Šķīdinātājs, smags nedegošs šķidrums - ugunsdzēšanas līdzeklis, iegūts, pilnībā hlorējot metānu: CH 4 +4Cl 2 3) citu alkānu mijiedarbība izraisa izomēru maisījuma veidošanās: CH 3 - CH 2 -CH 3 + 2Cl 2 → CH 3 ― CH 2 ― CH 2 Cl + + CH 3 ―CHCl― CH 3 + 2HCl | - | - | H +Br 2 halogenēšana H +HONO 2 ® nitrēšana | ||
| Pirolīze | C2H6CH2 = CH2+H2 | - | - | - | ||
| Izomerizācija | CH 3 – CH 2 – CH 2 – CH 3 ® | - | - | - | ||
| Pievienošanās reakcijas: -halogēni | - | CH 2 =CH 2 +Br 2 ® broma ūdens (vai broma šķīduma tetrahloretānā) atkrāsošana - kvalitatīva reakcija uz ogļūdeņražiem ar dubultsaiti | СНºСН +Br 2 ® BrСН= СНBr +Br 2 ® | - | ||
| - ūdeņradis (hidrogenēšana) | - | CH2=CH2+H2® | СНºСН ________® | +3H 2 benzols cikloheksāns | ||
| - ūdens (hidratācija) | - | CH2=CH2+H2O® | CHºCH + H 2 O ® | - | ||
| - halogenētie ogļūdeņraži | - | CH 2 = CH 2 + HCl ® | СНºСН + 2НCl ® | - | ||
| Polimkrizēšanas reakcija (BMC sintēze no mazmolekulāriem savienojumiem; NMC - monomērs, BMC - polimērs) | - | nCH2=CH2® | trimerizācija 3 CHºCH | - | ||
Ogļūdeņražu nosaukumi ir balstīti uzsistemātiska aizstāšanas nomenklatūra principi ir atspoguļoti diagrammā:
|
|
|
Nav paredzēts UV
alkāni alkēni alkēni alkīni
2. Piesātināto ogļūdeņražu nosaukums, kas ņemts par pamatu visu pārējo organisko savienojumu nosaukumiem ( saknes Grieķu cipari ir izcelti):
1. tabula.
| C atomu skaits | Vārds | C atomu skaits | Vārds | C atomu skaits | Vārds |
| C 1 | Met lv | C 7 | Hept lv | No 13 | Tridek lv |
| C 2 | Šis lv | No 8 | okt lv | No 20 | Eikoze lv |
| C 3 | Prop lv | No 9 | Nav lv | No 21 | Ģenikoze lv |
| C 4 | Booth lv | No 10 | decembris lv | No 22 | Dokoz lv |
| C 5 | Pent lv | No 11 | Undek lv | No 30 | Triacontan |
| C 6 | Hex lv | No 12 | Dodek lv | No 40 | Tetrakontāns |
2. tabula.Grieķu ciparu nosaukumi
ar kuru tas ir norādīts
identisku aizvietotāju skaits 3. tabula. Vietnieku vārdi
| Aizvietotāju skaits | Grieķu cipars | Aizvietotāju skaits | Grieķu cipars | vietnieks | Vārds |
| 2 | di- | 7 | hepta- | CH 3 - | Cl- |
| 3 | trīs- | 8 | astoņi | C 2 H 5 - | Br- |
| 4 | tetra- | 9 | nona- | C 3 H 7 - | es - |
| 5 | penta- | 10 | desmit- | F- | NH 2 - |
| 6 | heksa- |
3) Darbību secība, sastādot organisko ogļūdeņražu un to atvasinājumu nosaukumus.
A. Taisnas ķēdes ogļūdeņražu nosaukumi.
1. Alkānu nosaukumi doti 1. tabulā.
2. Alkēnu un alkīnu nosaukumu pamatā ir alkānu nosaukumi, kuros galotne –ane tiek aizstāta attiecīgi ar galotni –ene vai galotni –ine. Beigās mēs norādām daudzkārtējās saites pozīciju ar arābu ciparu.
B. Sazarotu ķēžu ogļūdeņražu nosaukumi.
1. Atrodiet galveno ķēdi:
2) Ietver dubulto, trīskāršo saiti,
3) Ietver tādus aizvietotājus kā F -, Cl -, Br -, I -.
2. Numurējam no gala, kuram tas ir vistuvāk
1) vietnieks
2) dubultās saites prioritāte palielinās
3) Trīskāršs savienojums no augšas uz leju
4) Alfabētiskā secībā mēs norādām aizvietotāju atrašanās vietu, izmantojot arābu ciparus (nosaukumus skatīt 3. tabulā).
5) Mēs dodam priekšroku opcijai, kurā pirmais atšķirīgais cipars ir mazākais.
6) Izmantojot prefiksu (skat. 2. tabulu), mēs norādām identisku aizvietotāju skaitu.
7) Pievienojiet galvenās ķēdes nosaukumu atbilstoši tajā esošo oglekļa atomu skaitam (sk. izceltās saknes 1. tabulā)
8) Alkēnu un alkīnu gadījumā nosaukuma beigās pievienojiet atbilstošu sufiksu –ene vai –ine.
9) Daudzkārtējā savienojuma vietu mēs norādām ar arābu ciparu (dodam priekšroku opcijai, kurā cipars ir mazākais).
C. Ievietojiet defisi starp cipariem un burtiem un komatu starp cipariem. Aromātisko ogļūdeņražu nosaukums ir balstīts uz tā vienkāršākā pārstāvja, benzola, nosaukumu.