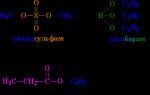Estrite füüsikalised omadused. Nomenklatuur ja isomeeria
Kui lähtehape on mitmealuseline, siis on võimalik kas täisestrite moodustumine - kõik HO rühmad on asendatud või happe estrid - osaline asendamine. Ühealuseliste hapete puhul on võimalikud ainult täisestrid (joonis 1).
Riis. 1. ESTRITE NÄITED anorgaanilise ja karboksüülhappe baasil
Estrite nomenklatuur.
Nimi luuakse järgmiselt: esiteks märgitakse happega seotud rühm R, seejärel happe nimi sufiksiga “at” (nagu anorgaaniliste soolade nimetustes: süsinik juures naatrium, nitraat juures kroom). Näited joonisel fig. 2

Riis. 2. ESTRITE NIMED. Molekulide fragmendid ja vastavad nimede fragmendid on esile tõstetud sama värviga. Estreid peetakse tavaliselt happe ja alkoholi vaheliste reaktsiooniproduktidena; näiteks butüülpropionaati võib pidada propioonhappe ja butanooli vahelise reaktsiooni tulemuseks.
Kui kasutate triviaalset ( cm. AINETE TRIVIALNE NIMETUS) lähtehappe nimetus, siis sisaldab ühendi nimetus sõna “ester”, näiteks C 3 H 7 COOC 5 H 11 - võihappe amüülester.
Estrite klassifikatsioon ja koostis.
Uuritud ja laialdaselt kasutatud estrite hulgas on enamus karboksüülhapetest saadud ühendeid. Mineraalsetel (anorgaanilistel) hapetel põhinevad estrid pole nii mitmekesised, sest mineraalhapete klass on vähemarvukas kui karboksüülhapped (ühendite mitmekesisus on üks orgaanilise keemia tunnuseid).
Kui C-aatomite arv algses karboksüülhappes ja alkoholis ei ületa 6–8, on vastavad estrid värvitud õlised vedelikud, enamasti puuviljalõhnaga. Nad moodustavad puuviljaestrite rühma. Kui estri moodustumisel osaleb aromaatne alkohol (sisaldab aromaatset tuuma), siis on sellistel ühenditel reeglina pigem lilleline kui puuviljalõhn. Kõik selle rühma ühendid on vees praktiliselt lahustumatud, kuid lahustuvad kergesti enamikes orgaanilistes lahustites. Need ühendid on huvitavad nende meeldivate lõhnade laia valiku tõttu (tabel 1), mõned neist eraldati algul taimedest ja sünteesiti hiljem kunstlikult.
| Tabel 1. MÕNED ESTRID, millel on puuvilja- või lillearoom (algsete alkoholide fragmendid liitvalemis ja nimes on paksus kirjas esile tõstetud) | ||
| Estri valem | Nimi | Aroom |
| CH 3 COO C4H9 | butüül atsetaat | pirn |
| C3H7COO CH 3 | Metüül Võihappe ester | õun |
| C3H7COO C2H5 | Etüül Võihappe ester | ananass |
| C 4 H 9 COO C2H5 | Etüül | karmiinpunane |
| C 4 H 9 COO C5H11 | Isoamil isovaleriinhappe ester | banaan |
| CH 3 COO CH2C6H5 | Bensüül atsetaat | jasmiin |
| C6H5COO CH2C6H5 | Bensüül bensoaat | lilleline |
Kui estrites sisalduvate orgaaniliste rühmade suurus suureneb C 15–30-ni, omandavad ühendid plastilise, kergesti pehmenevate ainete konsistentsi. Seda rühma nimetatakse vahadeks; need on tavaliselt lõhnatud. Mesilasvaha sisaldab erinevate estrite segu, üks vaha komponentidest, mis eraldati ja määrati koostis, on palmitiinhappe müritsüülester C 15 H 31 COOC 31 H 63. Hiina vaha (košenilli eritumise toode – Ida-Aasia putukad) sisaldab tseroothappe tserüülestrit C 25 H 51 COOC 26 H 53. Lisaks sisaldavad vahad ka vabu karboksüülhappeid ja alkohole, mis sisaldavad suuri orgaanilisi rühmi. Vahasid ei niisuta vesi ja need lahustuvad bensiinis, kloroformis ja benseenis.
Kolmas rühm on rasvad. Erinevalt kahest eelmisest ühehüdroksüülsetel alkoholidel ROH põhinevast rühmast on kõik rasvad estrid, mis on moodustunud kolmehüdroksüülsest alkoholist glütseroolist HOCH 2 – CH (OH) – CH 2 OH. Rasvadest koosnevatel karboksüülhapetel on tavaliselt 9–19 süsinikuaatomiga süsivesinikahel. Loomsed rasvad (lehmavõi, lambaliha, seapekk) on plastilised sulavad ained. Taimsed rasvad (oliivi-, puuvillaseemne-, päevalilleõli) on viskoossed vedelikud. Loomsed rasvad koosnevad peamiselt steariin- ja palmitiinhappe glütseriidide segust (joonis 3A, B). Taimeõlid sisaldavad veidi lühema süsinikuahela pikkusega hapete glütseriide: lauriin C 11 H 23 COOH ja mürist C 13 H 27 COOH. (nagu steariin- ja palmitiinhape, on need küllastunud happed). Selliseid õlisid saab pikka aega õhus säilitada, muutmata nende konsistentsi ja seetõttu nimetatakse neid mittekuivatavaks. Seevastu linaseemneõli sisaldab küllastumata linoolhappe glütseriidi (joonis 3B). Õhukese kihina pinnale kandmisel kuivab selline õli polümerisatsiooni käigus kaksiksidemetel õhuhapniku mõjul ning moodustub elastne kile, mis ei lahustu vees ja orgaanilistes lahustites. Looduslik kuivatusõli on valmistatud linaseemneõlist.

Riis. 3. STEARIIN- JA PALMITIHAPPE GLÜTSERIIDID (A JA B)– loomse rasva komponendid. Linoolhappe glütseriid (B) on linaseemneõli komponent.
Mineraalhapete estrid (alküülsulfaadid, madalamate alkoholide C1-8 fragmente sisaldavad alküülboraadid) on õlised vedelikud, kõrgemate alkoholide estrid (alates C9-st) on tahked ühendid.
Estrite keemilised omadused.
Karboksüülhapete estritele on kõige iseloomulikum estersideme hüdrolüütiline (vee mõjul) lõhustumine, neutraalses keskkonnas kulgeb see aeglaselt ja hapete või aluste juuresolekul märgatavalt kiireneb, kuna H + ja HO – ioonid katalüüsivad seda protsessi (joonis 4A), kusjuures hüdroksüülioonid toimivad tõhusamalt. Hüdrolüüsi leeliste juuresolekul nimetatakse seebistamiseks. Kui võtta kogu moodustunud happe neutraliseerimiseks piisav kogus leelist, toimub estri täielik seebistumine. See protsess viiakse läbi tööstuslikus mastaabis ning glütserool ja kõrgemad karboksüülhapped (C 15–19) saadakse leelismetallisoolade kujul, mis on seep (joonis 4B). Taimeõlides sisalduvate küllastumata hapete fragmendid, nagu kõik küllastumata ühendid, võivad olla hüdrogeenitud, vesinik kinnitub kaksiksidemetega ja moodustuvad loomsete rasvadega sarnased ühendid (joonis 4B). Seda meetodit kasutades toodetakse tööstuslikult päevalille-, soja- või maisiõli baasil tahkeid rasvu. Margariin on valmistatud taimsete õlide hüdrogeenimisproduktidest, mis on segatud looduslike loomsete rasvade ja erinevate toidulisanditega.

Peamine sünteesimeetod on karboksüülhappe ja alkoholi interaktsioon, mida katalüüsib hape ja millega kaasneb vee vabanemine. See reaktsioon on vastupidine joonisel fig. 3A. Et protsess kulgeks soovitud suunas (estri süntees), destilleeritakse (destilleeritakse) reaktsioonisegust vett. Märgitud aatomeid kasutavate spetsiaalsete uuringute abil õnnestus kindlaks teha, et sünteesi käigus eraldub happest (tähistatud punase punktiirraamiga) olev O-aatom, mis on osa saadud veest, mitte alkoholist ( realiseerimata valik on esile tõstetud sinise punktiirraamiga).
Sama skeemi abil saadakse anorgaaniliste hapete estrid, näiteks nitroglütseriin (joonis 5B). Hapete asemel võib kasutada happekloriide, meetod on rakendatav nii karboksüülhapete (joonis 5C) kui ka anorgaaniliste hapete (joonis 5D) puhul.
Karboksüülhappe soolade interaktsioon RCl halogeniididega viib samuti estrite tekkeni (joonis 5D), reaktsioon on mugav selle poolest, et see on pöördumatu – vabanenud anorgaaniline sool eemaldatakse koheselt orgaanilisest reaktsioonikeskkonnast sademe kujul.
Estrite kasutamine.
Tsellulooslakkide (nitrotselluloosi ja tselluloosatsetaadi baasil) lahustitena kasutatakse etüülformiaadi HCOOC 2 H 5 ja etüülatsetaati H 3 COOC 2 H 5.
Madalamatel alkoholidel ja hapetel põhinevaid estreid (tabel 1) kasutatakse toiduainetööstuses puuviljaessentside loomiseks, aromaatsete alkoholide baasil valmistatud estreid aga parfüümitööstuses.
Vahadest valmistatakse poleerimisvahendeid, määrdeaineid, immutuskompositsioone paberile (vahatatud paber) ja nahale, need sisalduvad ka kosmeetilistes kreemides ja ravimsalvides.
Rasvad koos süsivesikute ja valkudega moodustavad toitumiseks vajalike toiduainete komplekti, need on osa kõigist taime- ja loomarakkudest, lisaks täidavad nad kehas kogunedes energiavaru rolli. Tänu madalale soojusjuhtivusele kaitseb rasvakiht hästi loomi (eriti mereloomi – vaalu või morsaid) alajahtumise eest.
Loomsed ja taimsed rasvad on tooraine kõrgemate karboksüülhapete, detergentide ja glütserooli tootmiseks (joon. 4), mida kasutatakse kosmeetikatööstuses ja erinevate määrdeainete komponendina.
Nitroglütseriin (joonis 4) on tuntud ravim ja lõhkeaine, dünamiidi aluseks.
Kuivatusõlid on valmistatud taimeõlidest (joonis 3), mis on õlivärvide aluseks.
Väävelhappe estreid (joonis 2) kasutatakse orgaanilises sünteesis alküülivate (ühendisse alküülrühma sisseviimise) reagentidena ning fosforhappe estreid (joonis 5) kasutatakse putukamürkidena, samuti määrdeõlide lisandina.
Mihhail Levitski
Estrite olulisemad esindajad on rasvad.
Rasvad, õlid
Rasvad- need on glütserooli ja kõrgema üheaatomilisuse estrid. Selliste ühendite üldnimetus on triglütseriidid või triatsüülglütseroolid, kus atsüül on karboksüülhappe jääk -C(O)R. Looduslike triglütseriidide koostis sisaldab küllastunud hapete (palmitiinhape C 15 H 31 COOH, steariin C 17 H 35 COOH) ja küllastumata (oleiinhape C 17 H 33 COOH, linoolhape C 17 H 31 COOH) jääke. Kõrgematel karboksüülhapetel, mis on rasvade osa, on alati paarisarv süsinikuaatomeid (C 8 - C 18) ja hargnemata süsivesinike jääk. Looduslikud rasvad ja õlid on kõrgemate karboksüülhapete glütseriidide segud.
Rasvade koostist ja struktuuri saab kajastada üldvalemiga:

Esterdamine- estrite moodustumise reaktsioon.

Rasvade koostis võib sisaldada nii küllastunud kui ka küllastumata karboksüülhapete jääke erinevates kombinatsioonides.
Tavatingimustes on küllastumata hapete jääke sisaldavad rasvad enamasti vedelad. Neid nimetatakse õlid. Põhimõtteliselt on need taimset päritolu rasvad – linaseemne-, kanepi-, päevalille- ja muud õlid (erandiks on palmi- ja kookosõli – tavatingimustes tahked). Vähem levinud on loomset päritolu vedelad rasvad, näiteks kalaõli. Enamik loomse päritoluga looduslikke rasvu on tavatingimustes tahked (madalsulavad) ained ja sisaldavad peamiselt küllastunud karboksüülhapete jääke, näiteks lambarasv.
Rasvade koostis määrab nende füüsikalised ja keemilised omadused.
Rasvade füüsikalised omadused
Rasvad on vees lahustumatud, neil ei ole selget sulamistemperatuuri ja nende maht suureneb sulamisel oluliselt.
Rasvade agregaatolek on tahke, see on tingitud asjaolust, et rasvad sisaldavad küllastunud hapete jääke ja rasvamolekulid on võimelised tihedalt pakkima. Õlide koostis sisaldab cis-konfiguratsioonis küllastumata hapete jääke, seetõttu on molekulide tihe pakkimine võimatu ja agregatsiooni olek on vedel.
Rasvade keemilised omadused
Rasvad (õlid) on estrid ja neid iseloomustavad estrireaktsioonid.
On selge, et küllastumata karboksüülhapete jääke sisaldavate rasvade puhul on iseloomulikud kõik küllastumata ühendite reaktsioonid. Nad värvivad broomivett ja osalevad muudes liitumisreaktsioonides. Praktilises mõttes on kõige olulisem reaktsioon rasvade hüdrogeenimine. Tahked estrid saadakse vedelate rasvade hüdrogeenimisel. Just see reaktsioon on margariini – taimeõlidest saadud tahke rasva – tootmise aluseks. Tavaliselt saab seda protsessi kirjeldada reaktsioonivõrrandiga:

Kõik rasvad, nagu ka teised estrid, läbivad hüdrolüüsi:

Estrite hüdrolüüs on pöörduv reaktsioon. Hüdrolüüsiproduktide moodustumise tagamiseks viiakse see läbi leeliselises keskkonnas (leeliste või Na 2 CO 3 juuresolekul). Nendes tingimustes toimub rasvade hüdrolüüs pöörduvalt ja põhjustab karboksüülhapete soolade moodustumist, mida nimetatakse. leeliselises keskkonnas olevaid rasvu nimetatakse rasvade seebistamine.
Rasvade seebistamisel moodustuvad glütseriin ja seebid - kõrgemate karboksüülhapete naatriumi- ja kaaliumisoolad:
Seebistamine– rasvade aluseline hüdrolüüs, seebi tootmine.

Seep– kõrgemate küllastunud karboksüülhapete naatriumi (kaalium) soolade segud (naatriumseep - tahke, kaaliumseep - vedel).
Seebid on pindaktiivsed ained (lühendatult pindaktiivsed ained, pesuained). Seebi pesev toime tuleneb sellest, et seep emulgeerib rasvu. Seebid moodustavad saasteainetega mitselle (suhteliselt on need erinevate lisanditega rasvad).
Seebimolekuli lipofiilne osa lahustub saasteaines ja hüdrofiilne osa satub mitselli pinnale. Mitsellid laetakse ühtemoodi, seetõttu tõrjuvad ning saasteaine ja vesi muutuvad emulsiooniks (praktiliselt on tegu musta veega).

Seepi esineb ka vees, mis loob aluselise keskkonna.
Seepe ei saa kasutada kõvas või merevees, kuna tekkivad kaltsiumi (magneesiumi) stearaadid on vees lahustumatud.

Kui lähtehape on mitmealuseline, on võimalik kas täisestrite moodustumine, kõik HO rühmad on asendatud või happeestrite osaline asendamine. Ühealuseliste hapete puhul on võimalikud ainult täisestrid (joonis 1).
Riis. 1. ESTRITE NÄITED anorgaanilise ja karboksüülhappe baasil
Estrite nomenklatuur. Nimi luuakse järgmiselt: kõigepealt näidatakse rühm R , mis on happe külge kinnitatud, siis happe nimetus koos järelliitega “at” (nagu anorgaaniliste soolade nimetustes: süsinik juures naatrium, nitraat juures kroom). Näited joonisel fig.2
Kui kasutate triviaalset ( cm. VÄHESED AINETE NIMETUSED) on lähtehappe nimetus, siis sisaldab ühendi nimetus sõna “ester”, näiteks võihappe C 3 H 7 COOC 5 H 11 amüülester.
Estrite klassifikatsioon ja koostis. Uuritud ja laialdaselt kasutatud estrite hulgas on enamus karboksüülhapetest saadud ühendeid. Mineraalsetel (anorgaanilistel) hapetel põhinevad estrid pole nii mitmekesised, sest mineraalhapete klass on vähem arvukas kui karboksüülhapped (ühendite mitmekesisus on üks eristavaid tunnuseid orgaaniline keemia).Kui C-aatomite arv algses karboksüülhappes ja alkoholis ei ületa 68, on vastavad estrid värvitud õlised vedelikud, enamasti puuviljalõhnaga. Nad moodustavad puuviljaestrite rühma. Kui estri moodustumisel osaleb aromaatne alkohol (sisaldab aromaatset tuuma), siis on sellistel ühenditel reeglina pigem lilleline kui puuviljalõhn. Kõik selle rühma ühendid on vees praktiliselt lahustumatud, kuid lahustuvad kergesti enamikes orgaanilistes lahustites. Need ühendid on huvitavad nende meeldivate lõhnade laia valiku tõttu (tabel 1), mõned neist eraldati algul taimedest ja sünteesiti hiljem kunstlikult.
| Tabel 1. MÕNED ESTRID, millel on puuvilja- või lillearoom (algsete alkoholide fragmendid liitvalemis ja nimes on paksus kirjas esile tõstetud) | ||
| Estri valem | Nimi | Aroom |
| CH 3 COO C4H9 | butüül atsetaat | pirn |
| C3H7COO CH 3 | Metüül Võihappe ester | õun |
| C3H7COO C2H5 | Etüül Võihappe ester | ananass |
| C 4 H 9 COO C2H5 | Etüül | karmiinpunane |
| C 4 H 9 COO C5H11 | Isoamil isovaleriinhappe ester | banaan |
| CH 3 COO CH2C6H5 | Bensüül atsetaat | jasmiin |
| C6H5COO CH2C6H5 | Bensüül bensoaat | lilleline |
Kolmas rühm on rasvad. Erinevalt kahest eelmisest ühehüdroksüülsetel alkoholidel põhinevast rühmast
ROH , kõik rasvad on glütseroolalkoholi estrid HOCH 2 CH(OH)CH 2 OH. Rasvade moodustavatel karboksüülhapetel on reeglina 919 süsinikuaatomiga süsivesinikahel. Loomsed rasvad (lehmavõi, lambaliha, seapekk) plastik, sulavad ained. Taimsed rasvad (oliiv, puuvillaseemned, päevalilleõli) viskoossed vedelikud. Loomsed rasvad koosnevad peamiselt steariin- ja palmitiinhappe glütseriidide segust (joonis 3A, B). Taimeõlid sisaldavad veidi lühema süsinikuahela pikkusega hapete glütseriide: lauriin C 11 H 23 COOH ja mürist C 13 H 27 COOH. (nagu steariin ja palmitiinhape, on need küllastunud happed). Selliseid õlisid saab pikka aega õhus säilitada, muutmata nende konsistentsi ja seetõttu nimetatakse neid mittekuivatavaks. Seevastu linaseemneõli sisaldab küllastumata linoolhappe glütseriidi (joonis 3B). Õhukese kihina pinnale kandmisel kuivab selline õli polümerisatsiooni käigus kaksiksidemetel õhuhapniku mõjul ning moodustub elastne kile, mis ei lahustu vees ja orgaanilistes lahustites. Looduslik kuivatusõli on valmistatud linaseemneõlist.
Riis. 3. STEARIIN- JA PALMITIHAPPE GLÜTSERIIDID (A JA B) loomse rasva komponendid. Linoolhappe glütseriid (B) linaseemneõli komponent.
Mineraalhapete estrid (alküülsulfaadid, madalamate alkoholide fragmente sisaldavad alküülboraadid C 18) õlised vedelikud, kõrgemate alkoholide estrid (alates C 9) tahked ühendid.
Estrite keemilised omadused. Karboksüülhapete estritele on kõige iseloomulikum estersideme hüdrolüütiline (vee mõjul) lõhustumine, neutraalses keskkonnas kulgeb see aeglaselt ja hapete või aluste juuresolekul märgatavalt kiireneb, kuna H + ja HO ioonid katalüüsivad seda protsessi (joonis 4A), kusjuures hüdroksüülioonid toimivad tõhusamalt. Hüdrolüüsi leeliste juuresolekul nimetatakse seebistamiseks. Kui võtta kogu moodustunud happe neutraliseerimiseks piisav kogus leelist, toimub estri täielik seebistumine. See protsess viiakse läbi tööstuslikus mastaabis ning glütseriin ja kõrgemad karboksüülhapped (C 1519) saadakse leelismetallisoolade kujul, mis on seep (joonis 4B). Taimeõlides sisalduvate küllastumata hapete fragmendid, nagu kõik küllastumata ühendid, võivad olla hüdrogeenitud, vesinik kinnitub kaksiksidemetega ja moodustuvad loomsete rasvadega sarnased ühendid (joonis 4B). Seda meetodit kasutades toodetakse tööstuslikult päevalille-, soja- või maisiõli baasil tahkeid rasvu. Margariin on valmistatud taimsete õlide hüdrogeenimisproduktidest, mis on segatud looduslike loomsete rasvade ja erinevate toidulisanditega.Peamine sünteesimeetod on karboksüülhappe ja alkoholi interaktsioon, mida katalüüsib hape ja millega kaasneb vee vabanemine. See reaktsioon on vastupidine joonisel fig. 3A. Et protsess kulgeks soovitud suunas (estri süntees), destilleeritakse (destilleeritakse) reaktsioonisegust vett. Märgitud aatomeid kasutavate spetsiaalsete uuringute abil õnnestus kindlaks teha, et sünteesi käigus eraldub happest (tähistatud punase punktiirraamiga) olev O-aatom, mis on osa saadud veest, mitte alkoholist ( realiseerimata valik on esile tõstetud sinise punktiirraamiga).
Sama skeemi abil saadakse anorgaaniliste hapete estrid, näiteks nitroglütseriin (joonis 5B). Hapete asemel võib kasutada happekloriide, meetod on rakendatav nii karboksüülhapete (joonis 5C) kui ka anorgaaniliste hapete (joonis 5D) puhul.
Karboksüülhappe soolade interaktsioon alküülhalogeniididega
RCl viib ka estrite tekkeni (joonis 5D), reaktsioon on mugav selle poolest, et see on pöördumatu, vabanenud anorgaaniline sool eemaldatakse koheselt orgaanilisest reaktsioonikeskkonnast sademe kujul.Estrite kasutamine. Tsellulooslakkide (nitrotselluloosi ja tselluloosatsetaadi baasil) lahustitena kasutatakse etüülformiaadi HCOOC 2 H 5 ja etüülatsetaati H 3 COOC 2 H 5.Madalamatel alkoholidel ja hapetel põhinevaid estreid (tabel 1) kasutatakse toiduainetööstuses puuviljaessentside loomiseks, aromaatsete alkoholide baasil valmistatud estreid aga parfüümitööstuses.
Vahadest valmistatakse poleerimisvahendeid, määrdeaineid, immutuskompositsioone paberile (vahatatud paber) ja nahale, need sisalduvad ka kosmeetilistes kreemides ja ravimsalvides.
Rasvad koos süsivesikute ja valkudega moodustavad toitumiseks vajalike toiduainete komplekti, need on osa kõigist taime- ja loomarakkudest, lisaks täidavad nad kehas kogunedes energiavaru rolli. Rasvakiht kaitseb madala soojusjuhtivuse tõttu loomi (eriti merivaalasid või morsaid) hästi alajahtumise eest.
Loomsed ja taimsed rasvad on tooraine kõrgemate karboksüülhapete, detergentide ja glütserooli tootmiseks (joon. 4), mida kasutatakse kosmeetikatööstuses ja erinevate määrdeainete komponendina.
Nitroglütseriin (joonis 4) on tuntud ravim ja lõhkeaine, dünamiidi aluseks.
Kuivatusõlid on valmistatud taimeõlidest (joonis 3), mis on õlivärvide aluseks.
Väävelhappe estreid (joonis 2) kasutatakse orgaanilises sünteesis alküülivate (ühendisse alküülrühma sisseviimise) reagentidena ning fosforhappe estreid (joonis 5) kasutatakse putukamürkidena, samuti määrdeõlide lisandina.
Mihhail Levitski
KIRJANDUS Kartsova A.A. Aine vallutamine. Orgaaniline keemia. Kirjastus Khimizdat, 1999Pustovalova L.M. Orgaaniline keemia. Phoenix, 2003
Estrid sisaldavad funktsionaalset rühma:
kus R ja R" on samad või erinevad radikaalid.
Estreid võib pidada ka hapete derivaatideks, milles vesinikuaatom karboksüülrühmas on asendatud süsivesinikradikaaliga (R):
Füüsikalised omadused
Madalamate karboksüülhapete ja alkoholide estrid on lenduvad vees lahustumatud vedelikud. Paljudel neist on meeldiv lõhn. Näiteks butüülbutüraat lõhnab nagu ananass, isoamüülatsetaat lõhnab nagu pirn jne.
Kõrgemate rasvhapete ja alkoholide estrid on vahajad ained, lõhnatud ja vees lahustumatud. Lillede ja marjade meeldiv aroom on suuresti tingitud teatud estrite olemasolust neis.
Rasvad on looduses laialt levinud. Koos süsivesinike ja valkudega on nad osa kõigist taime- ja loomorganismidest ning moodustavad meie toidu ühe peamise osa.
Vastavalt nende toatemperatuuril agregeerumisastmele jagatakse rasvad vedelateks ja tahketeks. Tahked rasvad moodustavad reeglina küllastunud happed, vedelad rasvad (mida sageli nimetatakse õlideks) aga küllastumata happed. Rasvad lahustuvad orgaanilistes lahustites ja ei lahustu vees.
Estrite saamise põhimeetodid:
Esterdamine - karboksüülhapete ja alkoholide koostoime, näiteks etüülatsetaadi tootmine äädikhappest ja etüülalkoholist:
CH 3 COOH + C 2 H 5 OH = CH 3 COOC 2 H 5 + H 2 O
Keemilised omadused
1. Hüdrolüüsi või seebistamise reaktsioon.
Nagu eespool mainitud, on esterdamisreaktsioon pöörduv, seetõttu toimub hapete juuresolekul pöördreaktsioon, mida nimetatakse hüdrolüüsiks, mille tulemusena moodustuvad algsed rasvhapped ja alkohol:
Hüdrolüüsireaktsiooni katalüüsivad ka leelised; sel juhul on hüdrolüüs pöördumatu:
kuna saadud karboksüülhape moodustab leelisega soola:
CH 3 – COOH + NaOH → CH 3 – COONa + H 2 O
2. Lisamisreaktsioon.
Küllastumata hapet või alkoholi sisaldavad estrid on võimelised liituma. Näiteks katalüütilise hüdrogeenimise ajal lisavad nad vesinikku.
3. Taastumise reaktsioon.
Estrite redutseerimine vesinikuga põhjustab kahe alkoholi moodustumist:
4. Amiidide moodustumise reaktsioon.
Ammoniaagi mõjul muutuvad estrid happeamiidideks ja alkoholideks:
CH3-CO-O C2H5 + NH3 → CH3-CO-NH2 + C2H5OH.
56) Rasvad- need on estrite segud, mis on moodustunud kolmehüdroksüülsest alkoholiglütseroolist ja kõrgematest rasvhapetest. Rasvade üldvalem, kus R on kõrgemate rasvhapete radikaalid:
Kõige sagedamini sisaldab rasvade koostis küllastunud happeid: palmitiinhape C 15 H 31 COOH ja steariinhape C 17 H 35 COOH ning küllastumata happeid: oleiinhape C 17 H 33 COOH ja linoolhape C 17 H 31 COOH.
Glütserooliga karboksüülhapete ühendite üldnimetus on triglütseriidid.
Rasvade hüdrolüüs tehnoloogias (rasvade seebistamine). Rasvad on suure tehnilise tähtsusega: need on vajalikud materjalid seebi ja glütseriini tootmiseks. Seebid on kõrgemate rasvhapete soolad, mille lahused on puhastava toimega. Kõige levinumad on naatriumseebid, mida kasutatakse tehnikas ja igapäevaelus pesuainetena. Seebi valmistamise olemus on rasvade seebistamine kuumutamisel naatriumhüdroksiidi lahusega. Sel juhul lagundatakse rasvad glütseriiniks ja seebiks.
Rasvade hüdrolüüs ehk seebistamine toimub vee (pöörduv) või leeliste (pöördumatu) mõjul:
Niisiis: seebid on kõrgemate karboksüülhapete soolad. Tavapärased seebid koosnevad peamiselt palmitiin-, steariin- ja oleiinhappe soolade segust. Naatriumisoolad moodustavad tahkeid seepe, kaaliumisoolad vedelseepe.
Saadud glütseriini ja seebi segu eraldamiseks lisatakse naatriumkloriidi vesilahus, milles, nagu sama naatriumiooniga elektrolüüdis, lahustub seep väga halvasti. Selle tulemusena toimub delaminatsioon: peal on seebilahuse kiht ja allpool glütseriini ja naatriumkloriidi lahus. Seebilahus valatakse vormidesse, kus see taheneb. Glütserooli vesilahus aurustatakse, eraldatakse naatriumkloriidist ja puhastatakse destilleerimisega.
Seebi valmistamiseks kasutatakse erinevaid rasvu: seapekki, võid jne. Praegu kasutatakse seebi tootmiseks toiduks mittekasutatavat toorainet. Selleks vajalikud happed toodetakse tööstuslikus mastaabis parafiini moodustavate süsivesinike oksüdeerimise teel.
Keemilised omadused
1. Hüdrolüüs happelises keskkonnas
Rasvade pealekandmine
Rasvu kasutatakse toiduks. Osa õlisid kasutatakse kosmeetikatoodete (kreemid, maskid, salvid) valmistamiseks.
Mitmetel rasvadel on raviväärtus: kastoorõli, astelpajuõli, kalaõli, hanerasv.
Põllumajandusloomade söötmiseks kasutatakse heeringa kalaõli ja hülgeõli.
Kuivatusõlide tootmiseks kasutatakse taimeõlisid.
Margariini tootmise tooraineks on palju taimeõlisid ja vaalaõli.
Seebi- ja steariinküünalde tootmiseks kasutatakse loomseid rasvu.
Rasvu kasutatakse glütseriini ja määrdeainete tootmiseks.
1) Estrid – ______________________________________________________________________.
Estrid – __________________________________________________________________
__________________________________________________________________________________
__________________________________________________________________________________:
Kus R ja R / - _________________________________, mis võivad olla samad või erinevad.
Estrite funktsionaalset rühma nimetatakse ______________________________:
Estrite molekulaarset koostist väljendatakse üldvalemiga C - H - O -- .
2) Äädikhappe etüülester estrite esindajana.
3) Estrite nomenklatuur ja isomeeria
* Kui nimetada estrid näitavad IUPAC asendusnomenklatuuri reeglite kohaselt esmalt alkoholi alküülrühma nimetust ja seejärel happejäägi nimetust, asendades happe nimes oleva järelliide –ova järelliitega –oat.
Etüületanoaat
2-jääk 1-alküülrühm
happeline alkohol
* Struktuurne isomeeria
Klassi piires – ahela isomeeria:
Järgmised isomeerid vastavad molekulaarsele valemile C 4 H 8 O 2:
Etüületanoaat Propüülmetanoaat Metüülpropanoaat
Klassidevaheline isomeeria:
Etüületanoaat Butaanhape
4) Estrite hüdrolüüs
o happeline:
H2O + CH3-CH2-OH
_______________ _____________ ________
o Leeliseline:
NaOH + CH3-CH2-OH
______________ ______________ _________ ______________
5) Estrid looduses.
Palju estreid leidub looduslikult taimede lillede ja viljade rakumahlas.
Rasvad.
1) Triglütseriidide koostis ja struktuur.
Rasvad - ____________________________________________________________________________.
Rasvade põhikomponendid on ____________________ –__________________________
____________________________________________________________________________________.
Skeem, mis kajastab triglütseriidide üldist struktuuri:
Kus R1, R2, R3 on karboksüülhappe jäägid (____________ CH 3 CH 2 CH 2 COOH, ________________ C 15 H 31 COOH, _________________ C 17 H 35 COOH, ________________ C 17 H 33 COOH, ___1_7________ C 17 H 33 COOH, ___1_7__________ , ____________________________ C17H29COOH.
2) Füüsikalised omadused.
3) Rasvad kui toitained.
Rasvad on inimeste ja loomade toidu oluline osa. Kehas lagunevad hüdrolüüsi käigus rasvad glütserooliks ja kõrgemateks karboksüülhapeteks. Seejärel sünteesitakse rakkude sees hüdrolüüsiproduktidest konkreetsele organismile omased rasvad.
Rasvad on kõige olulisem energiaallikas: nende oksüdeerumisel tekib kaks korda rohkem energiat kui süsivesikute oksüdeerumisel.
Kodutöö: §§39-40, 42.
1. Looge reaktsioonivõrrandid, mida saab kasutada järgmiste teisenduste tegemiseks: C 2 H 6 ® C 2 H 6 ® C 2 H 5 OH ® CH 3 COOH ® CH 3 COO C 2 H 5
2. Koostage koostise C 5 H 10 O 2 kõigi võimalike isomeeride struktuurivalemid ja andke neile nimetused vastavalt IUPAC asendusnomenklatuuri reeglitele.
Loengud 20, 21 Süsivesinikud: alkaanid, alkeenid, alkeenid, areenid.
| Homoloogiliste seeriate nimetused Tunnused | Alkaanid | Alkeenid | Alküünid | Areenid | ||
| 1. Definitsioon | Atsüklilised küllastunud süsivesinikud, mille molekulides on süsinikuaatomid omavahel seotud ainult üksiksidemetega (lihtsidemetega) | Atsüklilised küllastumata süsivesinikud, mille molekulides on 2 süsinikuaatomit ühendatud kaksiksidemega | Atsüklilised küllastumata süsivesinikud, mille molekulides on kolmiksidemega seotud 2 süsinikuaatomit | Tsüklilised küllastumata süsivesinikud, mille molekulid sisaldavad ühte või mitut benseenitsüklit | ||
| 2. Üldvalem | C n H 2n+2 | CnH2n | CnH2n-2 | CnH2n-6 | ||
| 3. Lihtsaim esindaja | metaan | eteen | etiin | benseen | ||
| a) Molekulaarvalem | CH 4 | C2H4 | C2H2 | C6H6 | ||
| b) Struktuurivalem | H ½ H¾C¾H ½ H | H H\/C=C/\H H | H¾CºC¾H | |||
| c) Elektrooniline valem | ||||||
| 4. Molekuli ruumiline struktuur: a) Kuju | Metaan - tetraeedriline Metaani homoloogid, alustades butaanist - siksak | Topeltsideme piirkonnas - tasane | Kolmiksideme piirkonnas – silindriline (lineaarne) | Korter | ||
| b) Ühendusnurk | ||||||
| c) Ühenduse olemus | vallaline | kahekordne | kolmekordne | Aromaatne | ||
| d) sideme pikkus | 0,154 nm | 0,133 nm | 0,120 nm | 0,140 nm | ||
| 5. Süsinikuaatomite pöörlemise võimalus üksteise suhtes sõltuvalt sideme iseloomust | Suhteliselt tasuta | Seoses kaksiksidemega on see keeruline (võimatu ilma kaksiksidet purustamata) | Kolmiksideme puhul on see keeruline (ilma kolmiksidet purustamata on võimatu) | Benseenitsükli süsinikuaatomite vahel on takistatud (võimatu ilma benseenitsüklit purustamata) | ||
| 6. Triviaalsed nimed | C 1 metaan, C 2 etaan, C 3 propaan, C 4 butaan (lõpp -an, klassifitseeritud poolsüstemaatiliseks) | CH 2 = CH 2 etüleen, CH 2 = CH – CH 3 propüleen CH 2 = CH – CH 2 – CH 3 butüleen | CHºCH atsetüleen | C6C6benseen | ||
| 7. Isomerism – | sama kvalitatiivse ja kvantitatiivse koostisega, kuid erineva keemilise struktuuriga ühendite olemasolu nähtus (molekulis aatomite erinev ühendusjärjekord); süsivesinike puhul võib see olla struktuurne (ahelad; mitme sideme asukohad) ja ruumiline. | |||||
| Struktuurne | Ahela isomeeria | CH 3 – CH 2 – CH 2 – CH 3 t keemistemperatuur = -0,5°C CH 3 – CH– CH 3 ï CH 3 t keemistemperatuur = -1 0,2°C | CH 2 = CH – CH 2 – CH 3 buteen-1 CH 2 = C – CH 3 ï CH 3 2-metüülpropeen | CHºС CH 2 –CH 2 – CH 3 pentiin-1 CHºС – CH–– CH 3 ï CH 3 3-metüülbugiin-1 | - | |
| Mitme sideme positsiooni isomeeria | - | CH 2 =CH– CH 2 – CH 3 buteen-1 CH 3 –CH= CH– CH 3 buteen-2 | CHºС – CH 2 – CH 3 butiin-1 CH 3 –Сº С CH 3 butiin-2 | - | ||
| Ruumiline – cis-trans isomeeria | - | Н 3 С Н\ ¤ С=С ¤ \ Н 3 С Н cis-isomeer | H CH 3 \ ¤ C=C ¤ \ H 3 CH transisomeer | - | - | |
| Füüsikalised omadused | ||||||
| 1. füüsiline seisund: | C1-C4-_____, C5-C15-________, C16-____________________________; | C2-C4-______, C5-C17-______, C18-_______________________; | C2-C4-_____, C5-C16-_______, C17-_______________________; | vedelik (värvitu, väga murdumisvõimeline, iseloomuliku lõhnaga) | ||
| 2. t keema. ja t ujuvad. | M r suurenemisega t bp suureneb. ja t ujuvad. | M r suurenemisega t kip suureneb | t kip. = 80,1°С, t sula. =5,5°С | |||
| 3. vees lahustuvus | praktiliselt lahustumatu | praktiliselt lahustumatu | praktiliselt lahustumatu | lahustumatu | ||
| 4. füsioloogiline mõju organismile | - | - | - | väga mürgine ühend | ||
| Keemilised omadused | ||||||
| Oksüdatsioonireaktsioonid: - täielik oksüdatsioon (põlemine) - mittetäielik oksüdatsioon | CH 4 +2O 2 →______+____+Q Metaani segud hapnikuga (1:2 mahu järgi) ja õhuga (1:10) on plahvatusohtlikud 2CH 4 +3O 2 → | C 2 H 4 +_O 2 → C 2 H 4 + (O)+ H 2 O ® etüleenglükool | _C 2 H 2 +_O 2 → | _C 6 H 6 +__O 2 → | ||
| Asendusreaktsioonid (valgustuse all kloori ja broomiga) | 1) CH 4 +Cl 2 CH 3 ―CH 3 + Cl 2 → 2) Metaani halogeenimisel asenduvad järjestikku kõik vesinikuaatomid ja moodustub toodete segu: CH 4 CH 3 Cl metaan klorometaan → CH 2 Cl 2 CHCl 3 diklorometaan triklorometaan ( kloro- → CCl 4 roform) süsiniktetrakloriid (süsiniktetrakloriid) Lahusti, raske mittesüttiv vedelik - tulekustutus, saadakse metaani täielikul kloorimisel: CH 4 +4Cl 2 3) teiste alkaanide koostoime põhjustab isomeeride segu moodustumine: CH 3 - CH 2 -CH 3 + 2Cl 2 → CH 3 - CH 2 - CH 2 Cl + + CH 3 - CHCl - CH 3 + 2HCl | - | - | H +Br 2 halogeenimine H +HONO 2 ® nitreerimine | ||
| Pürolüüs | C2H6CH2 = CH2 + H2 | - | - | - | ||
| Isomerisatsioon | CH 3 – CH 2 – CH 2 – CH 3 ® | - | - | - | ||
| Lisamisreaktsioonid: -halogeenid | - | CH 2 =CH 2 +Br 2 ® broomivee (või broomi lahuse tetrakloroetaanis) värvitustamine - kvalitatiivne reaktsioon kaksiksidemega süsivesinikele | СНºСН +Br 2 ® BrСН= СНBr +Br 2 ® | - | ||
| - vesinik (hüdrogeenimine) | - | CH2=CH2+H2® | СНºСН ________® | +3H 2 benseen tsükloheksaan | ||
| - vesi (hüdratsioon) | - | CH2=CH2+H20® | CHºCH + H2O® | - | ||
| - halogeenitud süsivesinikud | - | CH2 = CH2 + HCl® | СНºСН + 2НCl ® | - | ||
| Polümriseerimisreaktsioon (BMC süntees madala molekulmassiga ühenditest; NMC - monomeer, BMC - polümeer) | - | nCH2=CH2® | trimerisatsioon 3 CHºCH | - | ||
Süsivesinike nimetused põhinevadsüstemaatiline asendusnomenklatuur kas skeemil kajastuvad põhimõtted:
|
|
|
Mitte UV jaoks
alkaanid alkaanid alkeenid alküünid
2. Küllastunud süsivesinike nimetus, mis on aluseks kõigi teiste orgaaniliste ühendite nimetustele ( juured Kreeka numbrid on esile tõstetud):
Tabel 1.
| C-aatomite arv | Nimi | C-aatomite arv | Nimi | C-aatomite arv | Nimi |
| C 1 | Meth et | C 7 | Hept et | Alates 13 | Tridek et |
| C 2 | See et | Alates 8 | okt et | Alates 20 | Eicosis et |
| C 3 | Prop et | Alates 9 | Mitte et | Alates 21 | Geneikoos et |
| C 4 | Booth et | Alates 10 | dets et | Alates 22 | Dokoz et |
| C 5 | Pent et | Alates 11 | Undek et | Alates 30 | Triacontan |
| C 6 | Hex et | Alates 12 | Dodek et | Alates 40 | Tetrakontaan |
Tabel 2.Kreeka numbrite nimed
millega see on näidatud
identsete asendajate arv Tabel 3. Asendusliikmete nimed
| Asendajate arv | Kreeka number | Asendajate arv | Kreeka number | asetäitja | Nimi |
| 2 | di- | 7 | hepta- | CH 3 - | Cl- |
| 3 | kolm- | 8 | kaheksa- | C2H5- | Br- |
| 4 | tetra- | 9 | mitte- | C3H7- | mina - |
| 5 | penta- | 10 | kümnend- | F- | NH 2 - |
| 6 | heksa- |
3) Toimingute järjekord orgaaniliste süsivesinike ja nende derivaatide nimetuste koostamisel.
A. Sirge ahelaga süsivesinike nimetused.
1. Alkaanide nimetused on toodud tabelis 1.
2. Alkeenide ja alküünide nimetused põhinevad alkaanide nimetustel, milles liide –ane on asendatud vastavalt sufiksiga –ene või sufiksiga –ine. Lõpus tähistame araabia numbriga mitmiksideme asukohta.
B. Hargnenud ahelaga süsivesinike nimetused.
1. Leidke põhiahel:
2) Sisaldab topelt-, kolmekordset sidet,
3) Sisaldab selliseid asendajaid nagu F-, Cl-, Br-, I-.
2. Nummerdame lõpust, millele see on kõige lähemal
1) asetäitja
2) Topeltsideme prioriteet suureneb
3) Kolmekordne ühendus ülalt alla
4) Tähestikulises järjekorras tähistame asendajate asukohad, kasutades araabia numbreid (nimed vt tabelist 3).
5) Eelistame valikut, mille puhul esimene erinev number on väikseim.
6) Prefiksi abil (vt tabel 2) näitame identsete asendajate arvu.
7) Lisage peaahela nimi vastavalt selles sisalduvate süsinikuaatomite arvule (vt esiletõstetud juured tabelis 1)
8) Alkeenide ja alküünide puhul lisa nime lõppu sobiv järelliide –een või –ine.
9) Märkame mitmekordse ühenduse asukoha araabia numbriga (eelistame valikut, mille puhul number on väikseim).
C. Asetage numbrite ja tähtede vahele sidekriips ning numbrite vahele koma. Aromaatsete süsivesinike nimetus põhineb selle lihtsaima esindaja benseeni nimel.